£Ø2013?ĒąµŗŅ»Ä££©Ģ¼”¢µŖŗĶĀĮµÄµ„ÖŹ¼°Ęä»ÆŗĻĪļŌŚ¹¤Å©ŅµÉś²śŗĶÉś»īÖŠÓŠÖŲŅŖµÄ×÷ÓĆ£®
£Ø1£©ÕęæÕĢ¼ČČ»¹Ō-ĀČ»Æ·ØæÉŹµĻÖÓÉĀĮæóÖʱø½šŹōĀĮ£¬ĘäĻą¹ŲµÄČČ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ
2Al
2O
3£Øs£©+2AlCl
3£Øg£©+6C£Øs£©ØT6AlCl£Øg£©+6CO£Øg£©”÷H=a kJ?mol
-13AlCl£Øg£©ØT2Al£Øl£©+AlCl
3£Øg£©”÷H=b kJ?mol
-1·“Ó¦Al
2O
3£Øs£©+3C£Øs£©ØT2Al£Øl£©+3CO£Øg£©µÄ”÷H=
0.5a+b
0.5a+b
kJ?mol
-1£ØÓĆŗ¬a”¢bµÄ“śŹżŹ½±ķŹ¾£©£»
£Ø2£©ÓĆ»īŠŌĢ滹Ō·ØæÉŅŌ“¦ĄķµŖŃõ»ÆĪļ£®Ä³ŃŠ¾æŠ”×éĻņijĆܱÕČŻĘ÷ÖŠ¼ÓČėŅ»¶ØĮæµÄ»īŠŌĢæŗĶNO£¬·¢Éś·“Ó¦C£Øs£©+2NO£Øg£©?N
2£Øg£©+CO
2£Øg£©”÷H=Q kJ?mol
-1£®ŌŚT
1”ꏱ£¬·“Ó¦½ųŠŠµ½²»Ķ¬Ź±¼ä²āµĆø÷ĪļÖŹµÄÅضČČēĻĀ£ŗ
Ź±¼ä£Ømin£©
ÅØ¶Č£Ømol/L£© |
0 |
10 |
20 |
30 |
40 |
50 |
| NO |
1.00 |
0.68 |
0.50 |
0.50 |
0.60 |
0.60 |
| N2 |
0 |
0.16 |
0.25 |
0.25 |
0.30 |
0.30 |
| CO2 |
0 |
0.16 |
0.25 |
0.25 |
0.30 |
0.30 |
¢Ł0”«10minÄŚ£¬NOµÄĘ½¾ł·“Ó¦ĖŁĀŹv£ØNO£©=
0.032mol?L-1?min-1
0.032mol?L-1?min-1
£¬T
1”ꏱ£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżK=
0.25
0.25
£»
¢Ś30minŗó£¬Ö»øıäijŅ»Ģõ¼ž£¬·“Ó¦ÖŲŠĀ“ļµ½Ę½ŗā£¬øł¾ŻÉĻ±ķÖŠµÄŹż¾ŻÅŠ¶ĻøıäµÄĢõ¼žæÉÄÜŹĒ
ad
ad
£ØĢī×ÖÄø±ąŗÅ£©£®
a£®ĶØČėŅ»¶ØĮæµÄNO b£®¼ÓČėŅ»¶ØĮæµÄ»īŠŌĢæ
c£®¼ÓČėŗĻŹŹµÄ“߻ƼĮ d£®ŹŹµ±ĖõŠ”ČŻĘ÷µÄĢå»ż
¢ŪČō30minŗóÉżøßĪĀ¶ČÖĮT
2”ę£¬“ļµ½Ę½ŗāŹ±£¬ČŻĘ÷ÖŠNO”¢N
2ӢCO
2µÄÅضČÖ®±ČĪŖ3£ŗ1£ŗ1£¬ŌņQ
£¼
£¼
0£ØĢī”°£¾”±»ņ”°£¼”±£©£®
¢ÜŌŚŗćČŻĢõ¼žĻĀ£¬ÄÜÅŠ¶ĻøĆ·“Ó¦Ņ»¶Ø“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŅĄ¾ŻŹĒ
bc
bc
£ØĢīŃ”Ļī±ąŗÅ£©£®
a£®µ„Ī»Ź±¼äÄŚÉś³É2nmol NO£Øg£©µÄĶ¬Ź±ĻūŗÄnmol CO
2£Øg£©
b£®·“Ó¦ĢåĻµµÄĪĀ¶Č²»ŌŁ·¢Éśøıä
c£®»ģŗĻĘųĢåµÄĆÜ¶Č²»ŌŁ·¢Éśøıä
d£®·“Ó¦ĢåĻµµÄŃ¹Ēæ²»ŌŁ·¢Éśøıä
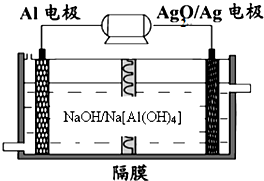
£Ø3£©ĀĮµē³ŲŠŌÄÜÓÅŌ½£¬Al-Ag
2Oµē³ŲæÉÓĆ×÷Ė®ĻĀ¶ÆĮ¦µēŌ“£¬ĘäŌĄķČēĶ¼ĖłŹ¾£ŗĒėŠ“³öøƵē³ŲÕż¼«·“Ó¦Ź½
Ag 2O+2e-+H2O=2Ag+2OH-
Ag 2O+2e-+H2O=2Ag+2OH-
£»³£ĪĀĻĀ£¬ÓĆøĆ»ÆѧµēŌ“ŗĶ¶čŠŌµē¼«µē½ā300mlĮņĖįĶČÜŅŗ£Ø¹żĮ棩£¬ĻūŗÄ27mg Al£¬Ōņµē½āŗóČÜŅŗµÄpH=
2
2
£Ø²»æ¼ĀĒČÜŅŗĢå»żµÄ±ä»Æ£©£®







 £Ø2013?ĒąµŗŅ»Ä££©Ģ¼”¢µŖŗĶĀĮµÄµ„ÖŹ¼°Ęä»ÆŗĻĪļŌŚ¹¤Å©ŅµÉś²śŗĶÉś»īÖŠÓŠÖŲŅŖµÄ×÷ÓĆ£®
£Ø2013?ĒąµŗŅ»Ä££©Ģ¼”¢µŖŗĶĀĮµÄµ„ÖŹ¼°Ęä»ÆŗĻĪļŌŚ¹¤Å©ŅµÉś²śŗĶÉś»īÖŠÓŠÖŲŅŖµÄ×÷ÓĆ£®
