
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
×ćĮæµÄĻĀĮŠĪļÖŹ·Ö±šÓėĶ¬Ģå»żĶ¬ÅØ¶ČµÄĻ”ĮņĖį·“Ó¦ŗó£¬ĖłµĆČÜŅŗµÄÖŹĮæ·ÖŹż×īŠ”µÄŹĒ””£Ø £©
AӢZn BӢZnO CӢZn(OH)2 DӢZnCO3
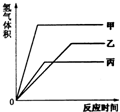 µČÖŹĮæµÄ¼×”¢ŅŅ”¢±ūČżÖÖ½šŹō£¬·Ö±šÓė×ćĮæµÄČÜÖŹÖŹĮæ·ÖŹżĻąĶ¬µÄĻ”ĮņĖįĶźČ«·“Ó¦ŗ󣬶¼Éś³É+2¼ŪµÄĮņĖįŃĪ£¬Ęä²śÉśĒāĘųµÄĢå»ż£ØĶ¬ĪĀĶ¬Ń¹£©Óė·“Ó¦Ź±¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
µČÖŹĮæµÄ¼×”¢ŅŅ”¢±ūČżÖÖ½šŹō£¬·Ö±šÓė×ćĮæµÄČÜÖŹÖŹĮæ·ÖŹżĻąĶ¬µÄĻ”ĮņĖįĶźČ«·“Ó¦ŗ󣬶¼Éś³É+2¼ŪµÄĮņĖįŃĪ£¬Ęä²śÉśĒāĘųµÄĢå»ż£ØĶ¬ĪĀĶ¬Ń¹£©Óė·“Ó¦Ź±¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©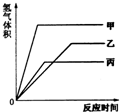 µČÖŹĮæµÄ¼×”¢ŅŅ”¢±ūČżÖÖ½šŹō£¬·Ö±šÓė×ćĮæµÄČÜÖŹÖŹĮæ·ÖŹżĻąĶ¬µÄĻ”ĮņĖįĶźČ«·“Ó¦ŗ󣬶¼Éś³É+2¼ŪµÄĮņĖįŃĪ£¬Ęä²śÉśĒāĘųµÄĢå»ż£ØĶ¬ĪĀĶ¬Ń¹£©Óė·“Ó¦Ź±¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
µČÖŹĮæµÄ¼×”¢ŅŅ”¢±ūČżÖÖ½šŹō£¬·Ö±šÓė×ćĮæµÄČÜÖŹÖŹĮæ·ÖŹżĻąĶ¬µÄĻ”ĮņĖįĶźČ«·“Ó¦ŗ󣬶¼Éś³É+2¼ŪµÄĮņĖįŃĪ£¬Ęä²śÉśĒāĘųµÄĢå»ż£ØĶ¬ĪĀĶ¬Ń¹£©Óė·“Ó¦Ź±¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(2)ČōÉčijpHµÄĮņĖįÖŠĖ®µēĄė³öµÄc(H£«)£½1.0”Į10£amol”¤L£1£¬ÉčĻąĶ¬pHµÄĮņĖįĀĮÖŠĖ®µēĄė³öµÄc(H+)£½1.0”Į10£b mol”¤L£1(a”¢b¶¼ŹĒŠ”ÓŚ14µÄÕżŹż)£¬ÄĒĆ“aŗĶbÖ®¼äĀś×ćµÄŹżĮæ¹ŲĻµŹĒ(ÓĆŅ»øöµČŹ½ŗĶŅ»øö²»µČŹ½±ķŹ¾)__________________£¬________________”£
(3)¹ĢĢåAµÄ»ÆѧŹ½ĪŖNH5£¬ĖüµÄĖłÓŠŌ×ÓµÄ×īĶā²ć¶¼·ūŗĻĻąÓ¦µÄĻ”ÓŠĘųĢåŌ×ÓµÄ×īĶā²ćµē×Ó½į¹¹£¬ŌņAµÄµē×ÓŹ½ĪŖ_________________________”£
0£ŗÓŠĖÄÖÖÖŹĮæ±ČæÉÄÜĻąĶ¬»ņ²»Ķ¬µÄĆ¾ĀĮŗĻ½šŃłĘ·¢Ł”¢¢Ś”¢¢Ū”¢¢Ü”£¼×”¢ŅŅ”¢±ū”¢¶”ĖÄĶ¬Ń§ø÷Č”Ņ»ÖÖѳʷ£¬½ųŠŠĻĀĮŠŹµŃ飬ĒóŗĻ½šÖŠĆ¾µÄÖŹĮæ·ÖŹż”£
(I)¼×Ȕѳʷ¢Łm1gŗĶ¹żĮæµÄĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦£¬Č»ŗó¹żĀĖ£»ŌŁĶłĀĖŅŗÖŠĶØČė¹żĮæµÄ¶žŃõ»ÆĢ¼ĘųĢ壬½«ĖłµĆ³Įµķ¹żĀĖ”¢Ļ“µÓ”¢ŗęøÉ”¢×ĘÉÕ£¬µĆµ½¹ĢĢåÖŹĮæČŌĪŖm1g”£ŌņŗĻ½šÖŠĆ¾µÄÖŹĮæ·ÖŹżĪŖ_______________________”£
(II)ŅŅȔѳʷ¢Śm2gŗĶ×ćĮæµÄŃĪĖį·“Ó¦£¬Č»ŗóµĪ¼Ó¹żĮæµÄĒāŃõ»ÆÄĘČÜŅŗ£¬½«³Įµķ¹żĀĖ”¢Ļ“µÓ”¢ŗęøÉ”¢×ĘÉÕ£¬µĆµ½¹ĢĢåÖŹĮæČŌĪŖm2g”£ŌņŗĻ½šÖŠĆ¾µÄÖŹĮæ·ÖŹżĪŖ_______________________”£
(III)±ūȔѳʷ¢Ūm3gŗĶ×ćĮæµÄĻ”ĮņĖį·“Ó¦£¬·¢ĻÖ¹ĢĢåĶźČ«Čܽā£¬±ź×¼×“æöĻĀµĆµ½ĘųĢåĢå»żĪŖVL£¬Ōņm3µÄȔֵ·¶Ī§ŹĒ___________________”£
(IV)¶”Č”²»Ķ¬ÖŹĮæµÄѳʷ¢Ü·Ö±šŗĶ30 mLĶ¬ÅØ¶ČµÄŃĪĖį·“Ó¦£¬ĖłČ”ŗĻ½šÖŹĮæÓė²śÉśĘųĢåĢå»ż(±ź×¼×“æöĻĀ²ā¶Ø)ČēĻĀ±ķĖłŹ¾£ŗ
ŹµŃéŠņŗÅ | a | b | c |
ŗĻ½šÖŹĮæ(mg) | 510 | 765 | 918 |
ĘųĢåĢå»ż( mL) | 560 | 672 | 672 |
Ēó£ŗ(1)ŌņŃĪĖįµÄĪļÖŹµÄĮæÅØ¶Č£»(2)ŗĻ½šÖŠĆ¾µÄÖŹĮæ·ÖŹż£» (3)ŌŚc×鏵Ńéŗ󣬻¹ŠčĻņČŻĘ÷ÖŠ¼ÓČė1.0 mol/LµÄĒāŃõ»ÆÄĘČÜŅŗ¶ąÉŁŗĮÉż²ÅÄÜŹ¹Ź£ÓąŗĻ½šÖŠµÄĀĮĒ”ŗĆĶźČ«Čܽā
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com