
题目列表(包括答案和解析)
(12分 )水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子中氧原子在基态时核外电子排布式为_ __;
(2)写出与H2O分子互为等电子体的微粒____(填1种)。
(3)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是_____
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
第 6 页 共 8 页
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
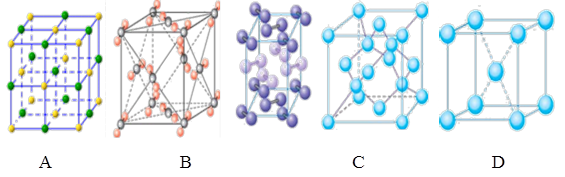
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是_____(请用相应的编号填写)
(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是_________kJ/mol;
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。
请写出生成此配合离子的离子方程式:___ 。
(12分 )水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子中氧原子在基态时核外电子排布式为_ __;
(2)写出与H2O分子互为等电子体的微粒____(填1种)。
(3)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是_____
| A.氧原子的杂化类型发生了改变 |
| B.微粒的形状发生了改变 第 6页 共 8页 |
| C.微粒的化学性质发生了改变 |
| D.微粒中的键角发生了改变 |

(12分 )水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
(1)水分子中氧原子在基态时核外电子排布式为_ __;
(2)写出与H2O分子互为等电子体的微粒____(填1种)。
(3)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是_____
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
第 6 页 共 8 页
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是_____(请用相应的编号填写)

(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是_________kJ/mol;
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。
请写出生成此配合离子的离子方程式:___ 。
(12分)氧化还原反应知识的学习,为我们研究化学物质和化学反应提供了新的视角。 (1)在氧化还原反应中,氧化剂 电子,发生 反应。
(2)理论上,处于最低价态的元素通常具有 性,在氧化还原反应中常作 剂。
(3)下列物质在氧化还原反应中,常作还原剂的有 ;常作氧化剂的有 (均填序号)。
①KmnO4②铝③氯水④FeCl3⑤一氧化碳⑥Na2S
(4)钠 与水反应的化学方程式为 。
与水反应的化学方程式为 。
铁与水反应的化学方程式为 ;在该反应中,若消耗3mol Fe,则转移的电子为( ) mol。
Fe,则转移的电子为( ) mol。
事实证明,钠的还原性比铁的还原性(填“强”或“弱”) 。
(12分)某化学兴趣小组的同学用下图所示实验装置进行实验研究(图中a、b、c表示止水夹).请对其方案进行完善或评价;
(1)实验室将B、C、E相连后,以 、 (填写名称)为原料可制取Cl2,为接下来研究氯气的化学性质做准备。
(2) 利用实验室常用方法制取氯气,将A、C、E相连,在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
| 实验 序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气 泡产生 | 氯气与水反应的产物具有酸性 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com