
题目列表(包括答案和解析)
(1)试推算“偏二甲肼”的分子式_________,并写出它的结构简式_________。
(2)写出燃料燃烧的热化学方程式:____________________________。
火箭的主要燃料是“偏二甲肼”,已知该化合物由C.H、N三种元素组成, WC=40%,WH=13.33%,其分子量为60。通过结构分析可知,该物质分子中其中有一个氮原子以 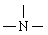 存在,且不与H原子直接相连。燃料的氧化剂是N2O4,燃烧产物只有CO2、H2O、N2;5.00g“偏二甲肼”完全燃烧时可放出212.5kJ热量。
存在,且不与H原子直接相连。燃料的氧化剂是N2O4,燃烧产物只有CO2、H2O、N2;5.00g“偏二甲肼”完全燃烧时可放出212.5kJ热量。
(1)试推算“偏二甲肼”的分子式,并写出它的结构简式。
(2)写出燃料燃烧的热化学方程式。
火箭的主要燃料是“偏二甲肼”,已知该化合物由C.H、N三种元素组成, WC=40%,WH=13.33%,其分子量为60。通过结构分析可知,该物质分子中其中有一个氮原子以 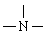 存在,且不与H原子直接相连。燃料的氧化剂是N2O4,燃烧产物只有CO2、H2O、N2;5.00g“偏二甲肼”完全燃烧时可放出212.5kJ热量。
存在,且不与H原子直接相连。燃料的氧化剂是N2O4,燃烧产物只有CO2、H2O、N2;5.00g“偏二甲肼”完全燃烧时可放出212.5kJ热量。
(1)试推算“偏二甲肼”的分子式,并写出它的结构简式。
(2)写出燃料燃烧的热化学方程式。
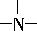 存在,且不与H原子直接相连。燃料的氧化剂是N2O4,燃烧产物只有CO2、H2O、N2,5.00g“偏二甲胼”完全燃烧时可放出212.5kJ热量。
存在,且不与H原子直接相连。燃料的氧化剂是N2O4,燃烧产物只有CO2、H2O、N2,5.00g“偏二甲胼”完全燃烧时可放出212.5kJ热量。 存在,且不与H原子直接相连。燃料的氧化剂是N2O4,燃烧产物只有CO2、H2O、N2;5.00g“偏二甲肼”完全燃烧时可放出212.5kJ热量。
存在,且不与H原子直接相连。燃料的氧化剂是N2O4,燃烧产物只有CO2、H2O、N2;5.00g“偏二甲肼”完全燃烧时可放出212.5kJ热量。湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com