
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)


| ||
| ||
| ||
| ||

| X-Y | X=Y | XЁдY | |
| BDЕФМќФмЃЈkJ?mol-1ЃЉ | 357.7 | 798.9 | 1071.9 |
| C2ЕФМќФмЃЈkJ?mol-1ЃЉ | 154.8 | 418.4 | 941.7 |
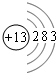
ЃЈ10ЗжЃЉAЁЂBЁЂCЁЂDЫФжждЊЫиЕФдзгађЪ§ОљаЁгк18ЃЌЦфзюИпе§МлЪ§вРДЮЮЊ1ЃЌ4ЃЌ5ЃЌ7ЃЌвбжЊBЕФдзгКЫЭтДЮЭтВуЕчзгЪ§ЮЊ2ЁЃAЁЂCдзгЕФКЫЭтДЮЭтВуЕчзгЪ§ЮЊ8ЁЃDдЊЫиЕФзюИпМлбѕЛЏЮяЖдгІЕФЫЎЛЏЮяЪЧвбжЊКЌбѕЫсжазюЧПЫсЃЌдђЃК
ЃЈ1ЃЉAЕФРызгНсЙЙЪОвтЭМЪЧ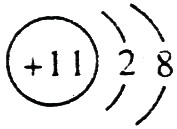 ЃЌCЕФдзгНсЙЙЪОвтЭМЪЧ
ЃЌCЕФдзгНсЙЙЪОвтЭМЪЧ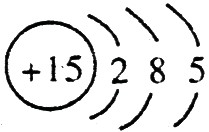 ЁЃ
ЁЃ
ЃЈ2ЃЉCЕФзюИпМлбѕЛЏЮяЖдгІЕФЫЎЛЏЮягыAЕФЧтбѕЛЏЮяЩњГЩШ§жжбЮЃЌЛЏбЇЪНЗжБ№ЮЊNa3PO4ЁЂNa2HPO4ЁЂNaH2PO4ЁЃ
ЃЈ3ЃЉCЁЂDЕФЦјЬЌЧтЛЏЮяЮШЖЈадгЩЧПЕНШѕЕФЫГађЪЧ HClЃОPH3ЁЃ
ЁОНтЮіЁП зюИпе§МлЃНдзгзюЭтВуЕчзгЪ§ЃЌBдЊЫиЕФдзгзюЭтВуЕчзгЪ§гІЮЊ4ЃЌBдЊЫидзгЕФДЮЭтВуЕчзгЪ§ЮЊ2ЃЌЮЊKВуЃЌBдЊЫидзгКЫЭтЙВга2ЃЋ4ЃН6ИіЕчзгЃЌBЪЧ6КХдЊЫиЬМЃЛAЁЂCдзгДЮЭтВуЕчзгЪ§ЮЊ8ЃЌдђAЁЂCдзгКЫЭтЕчзгЪ§ЗжБ№ЪЧЃК2ЃЋ8ЃЋ1ЃН11КЭ2ЃЋ8ЃЋ5ЃН15ЃЌЫљвдAЮЊ11КХдЊЫиФЦЃЌCЮЊ15КХдЊЫиСзЃЛдк1ЁЋ18КХдЊЫижаЃЌзюИпМлЮЊЃЋ7ЕФжЛгаТШдЊЫиЃЈFЮое§МлЃЉЃЌЖјHClO4ЪЧвбжЊКЌбѕЫсжазюЧПЕФЫсЃЌЙЪDЮЊТШЁЃ
ЃЈ1ЃЉФЦзмЪЧЃЋ1МлЃЌЦфРызгНсЙЙЪОвтЭМЮЊЃК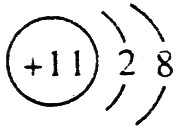 ЃЛСзЕФдзгађЪ§ЪЧ15ЃЌЦфдзгНсЙЙЪОвтЭМЪЧЃК
ЃЛСзЕФдзгађЪ§ЪЧ15ЃЌЦфдзгНсЙЙЪОвтЭМЪЧЃК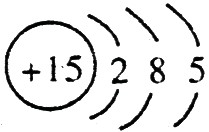 ЁЃ
ЁЃ
ЃЈ2ЃЉСзЕФзюИпМлЃЈЃЋ5ЃЉбѕЛЏЮяЖдгІЕФЫЎЛЏЮяЪЧH3PO4ЃЌгыNaOHЗДгІЩњГЩЃКNa3PO4ЁЂNaH2PO4Ш§жжбЮЁЃ
ЃЈ3ЃЉPЁЂClдзгЖМОпга3ИіЕчзгВуЃЌКЫЕчКЩЪ§P(15)аЁгкCl(17)ЃЌдзгАыОЖr(P)ЃОr(Cl)ЃЌЫљвдЗЧН№ЪєClЃОPЃЌЦјЬЌЧтЛЏЮяЮШЖЈадHClЃОPH3ЁЃ
ЃЈ11ЗжЃЉAЁЂBЁЂCЁЂDЁЂEЮЊдЊЫижмЦкБэжаЧАШ§жмЦкдЊЫиаЮГЩЕФЮхжжРызгЃЌAЁЂBЁЂCЁЂDЫФжжРызгЕФЕчзгЪ§ОљБШEЕФЕчзгЪ§Щй8.
ЃЈ1ЃЉAгыBНсКЯГЩЕФЛЏКЯЮяМзжаМШгаРызгМќгжгаЙВМлМќЃЌAгыCНсКЯГЩЕФЛЏКЯЮяввФбШмгкЫЎЃЌввШмгкМзЕФЫЎШмвКЕУЮоЩЋЭИУїШмвКЃЌCдЊЫидкжмЦкБэжаЕФЮЛжУЮЊ________________ввгыМзЕФЫЎШмвКЗДгІЕФРызгЗНГЬЪНЮЊ_______________________________________ЃЎ
ЃЈ2ЃЉBгыEНсКЯГЩЛЏКЯЮяБћЃЌЦфжаРызгЪ§жЎБШЮЊ2ЁУ1ЃЌAгыDНсКЯГЩЛЏКЯЮяЖЁЃЌЖЁгыБћЗДгІВњЩњЮоЩЋЮоЮЖЕФЦјЬхЃЌИУЗДгІЕФЛЏбЇЗНГЬЪНЮЊ ______________________
ЃЈ3ЃЉгавЛжжвКЬЌЕЊЧтЛЏКЯЮяЮьЃЌЗжзгжаЕЊгыЧтСНжждЊЫиЕФжЪСПБШЮЊ7ЁУ1ЃЌгыEЕФЕчзгЪ§ЯрЭЌЃЌЪЧЁАЩёжлЦпКХЁБЗЩДЌЗЂЩфЪБЪЙгУЕФИпФмШМСЯжЎвЛЃЌНсЙЙЗжЮіЗЂЯжИУЗжзгНсЙЙжажЛгаЕЅМќЃЌгыАБЯрЫЦЃЌдђЮьЕФНсЙЙЪНЮЊ_____________ЃЌ1 molЮьгыЙ§СПбЮЫсЗДгІЕФРызгЗНГЬЪНЪЧ ________________________ ЮьдкбѕЛЏЛЙдЗДгІжагыH2O2ЯрЫЦЃЌМШПЩзїбѕЛЏМСЃЌгжПЩзїЛЙдМСЃЌИљОнМлЬЌЗжЮіВњЩњетжжЧщПіЕФдвђЪЧ_______________________________________________________________ЃЛ8 gвКЬЌЮьгывКЬЌЫЋбѕЫЎЧЁКУЭъШЋЗДгІЃЌВњЩњСНжжЮоЖОгжВЛЮлШОЛЗОГЕФЦјЬЌЮяжЪЃЌЗХГі375 kJЕФШШСПЃЌаДГіИУЗДгІЕФШШЛЏбЇЗНГЬЪН
________________________________________________________________
ЃЈ11ЗжЃЉAЁЂBЁЂCЁЂDЁЂEЮЊдЊЫижмЦкБэжаЧАШ§жмЦкдЊЫиаЮГЩЕФЮхжжРызгЃЌAЁЂBЁЂCЁЂDЫФжжРызгЕФЕчзгЪ§ОљБШEЕФЕчзгЪ§Щй8.
ЃЈ1ЃЉAгыBНсКЯГЩЕФЛЏКЯЮяМзжаМШгаРызгМќгжгаЙВМлМќЃЌAгыCНсКЯГЩЕФЛЏКЯЮяввФбШмгкЫЎЃЌввШмгкМзЕФЫЎШмвКЕУЮоЩЋЭИУїШмвКЃЌCдЊЫидкжмЦкБэжаЕФЮЛжУЮЊ________________ввгыМзЕФЫЎШмвКЗДгІЕФРызгЗНГЬЪНЮЊ_______________________________________ЃЎ
ЃЈ2ЃЉBгыEНсКЯГЩЛЏКЯЮяБћЃЌЦфжаРызгЪ§жЎБШЮЊ2ЁУ1ЃЌAгыDНсКЯГЩЛЏКЯЮяЖЁЃЌЖЁгыБћЗДгІВњЩњЮоЩЋЮоЮЖЕФЦјЬхЃЌИУЗДгІЕФЛЏбЇЗНГЬЪНЮЊ ______________________
ЃЈ3ЃЉгавЛжжвКЬЌЕЊЧтЛЏКЯЮяЮьЃЌЗжзгжаЕЊгыЧтСНжждЊЫиЕФжЪСПБШЮЊ7ЁУ1ЃЌгыEЕФЕчзгЪ§ЯрЭЌЃЌЪЧЁАЩёжлЦпКХЁБЗЩДЌЗЂЩфЪБЪЙгУЕФИпФмШМСЯжЎвЛЃЌНсЙЙЗжЮіЗЂЯжИУЗжзгНсЙЙжажЛгаЕЅМќЃЌгыАБЯрЫЦЃЌдђЮьЕФНсЙЙЪНЮЊ_____________ЃЌ1 molЮьгыЙ§СПбЮЫсЗДгІЕФРызгЗНГЬЪНЪЧ ________________________ ЮьдкбѕЛЏЛЙдЗДгІжагыH2O2ЯрЫЦЃЌМШПЩзїбѕЛЏМСЃЌгжПЩзїЛЙдМСЃЌИљОнМлЬЌЗжЮіВњЩњетжжЧщПіЕФдвђЪЧ_______________________________________________________________ЃЛ8 gвКЬЌЮьгывКЬЌЫЋбѕЫЎЧЁКУЭъШЋЗДгІЃЌВњЩњСНжжЮоЖОгжВЛЮлШОЛЗОГЕФЦјЬЌЮяжЪЃЌЗХГі375 kJЕФШШСПЃЌаДГіИУЗДгІЕФШШЛЏбЇЗНГЬЪН
________________________________________________________________
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com