
题目列表(包括答案和解析)
(共12分) 工业上以锂辉石(Li2O·Al2O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下:
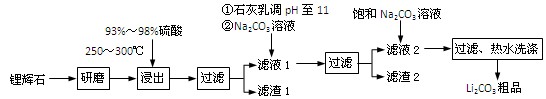
已知:① Li2O·Al2O3·4SiO2 H2SO4(浓)
H2SO4(浓) Li2SO4
Li2SO4 Al2O3·4SiO2·H2O↓
Al2O3·4SiO2·H2O↓
② 某些物质的溶解度(S)如下表所示:
|
T/℃ |
20 |
40 |
60 |
80 |
|
|
1.33 |
1.17 |
1.01 |
0.85 |
|
|
34.2 |
32.8 |
31.9 |
30.7 |
③ 从滤渣1中分离出Al2O3的部分流程如下图所示:

(1)、请依次写出在括号内加入试剂的化学式 、 。
(2)、请依次写出方框中所得到物质的化学式 、 。
(3)、步骤Ⅰ中反应的离子方程式是 。
(4)、已知滤渣2的主要成分有Mg(OH)2和CaCO3。向滤液1中加入石灰乳的作用是(运用化学平衡原理简述) 。
(5)、向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是
。
(6)、氧化铝在工业上用作高温耐火材料,制耐火砖、坩埚、瓷器、人造宝石等,同时氧化铝也是炼铝的原料。写出用氧化铝炼铝的化学方程式: 。
(第一个空1分,其它每空2分,共9分)有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同。
回答下列问题:
(1)B的元素名称为 ,D在周期表中的位置 。
(2)A,C,D对应的离子半径由大到小顺序为 ,(用化学符号表示)
(3)D的单质与水反应的离子方程式为_ 。
(4)向D与E形成的化合物的水溶液中滴入过量烧碱溶液,用离子方程式表述
。
(第一个空1分,其它每空2分,共9分)有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同。
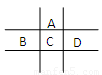
回答下列问题:
(1)B的元素名称为 ,D在周期表中的位置 。
(2)A,C,D对应的离子半径由大到小顺序为 ,(用化学符号表示)
(3)D的单质与水反应的离子方程式为_ 。
(4)向D与E形成的化合物的水溶液中滴入过量烧碱溶液,用离子方程式表述
。
(第一个空1分,其它每空2分,共9分)有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同。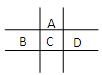
回答下列问题:
(1)B的元素名称为 ,D在周期表中的位置 。
(2)A,C,D对应的离子半径由大到小顺序为 ,(用化学符号表示)
(3)D的单质与水反应的离子方程式为_ 。
(4)向D与E形成的化合物的水溶液中滴入过量烧碱溶液,用离子方程式表述
。
(9分)有一离子晶体经测定属立方晶系,晶胞参数a=4.00Å(1Å=10-8cm),晶胞的顶点位置为Mg2+,体心位置为K+,所有棱边中点为F-。
(1) 该晶体的化学组成是 ;
(2) 晶胞类型是 ;
(3) Mg2+的F-配位数是 ,K+的F-配位数是 ;
(4) 该晶体的理论密度是 g?cm-3。
(5) 设晶体中正离子和负离子互相接触,已知F-的离子半径为1.33Å,试估计Mg2+的离子半径是 Å,K+的离子半径是 Å。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com