
题目列表(包括答案和解析)
1.[化学—有机化学基础]
下列框图表示A、B、C、D、E、F、G、H、I各物质间的转化关系,已知有机物H分子中含有5个碳原子。有机物I是一种高分子材料。

已知R—CN![]() R—COOH
R—COOH
请回答下列问题:
(1)物质D和I的结构简式为:
D___________________,
I__________________。
(2)指出反应类型:反应④属___________,⑥属___________。
(3)写出下列反应的化学方程式:
反应②_______________________________________________________________。
反应⑦_______________________________________________________________。
(4)写出与H具有相同官能团且只含有一个甲基的同分异构体的结构简式(除H外,请写出任意两种)________________________,________________________。
2.[化学—物质结构与性质]
今有位于元素周期表短周期中的X、Y、Z三种元素。已知:
①三者原子序数之和为25;
②元素Y的原子价电子排布为ns2npn+2;
③X和Y在不同条件下可形成X2Y和X2Y2两种固态化合物,Y和Z在不同条件下可形成ZY和ZY2两种气态化合物;
④元素Z的硫化物与元素Z的氯化物,常温下均为液态,且二者的相对分子质量之比为38∶77。
据此填写下列空白:
(1)写出元素符号:
X____________;Y____________;Z____________。
(2)X2Y2属于___________晶体,构成晶体的微粒是________________(填微粒符号)。
(3)Z的硫化物的分子空间构型是_________________________,ZY2形成的晶体属于______________________晶体,根据原子轨道重叠方式的不同,Z的氯化物分子中含有的共价键种类及数目是__________________________。
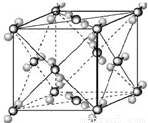
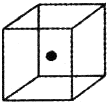
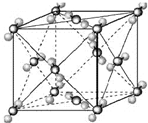 (2009?宿迁模拟)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中B、D、E原子最外电子层的p能级(轨道)上的电子处于半满状态.通常情况下,A的一种氧化物分子为非极性分子,其晶胞结构如右下图所示.原子序数为31的元素镓(Ga)与元素B形成的一种化合物是继以C单质为代表的第一代半导体材料和GaE为代表的第二代半导体材料之后,在近10年迅速发展起来的第三代新型半导体材料.
(2009?宿迁模拟)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中B、D、E原子最外电子层的p能级(轨道)上的电子处于半满状态.通常情况下,A的一种氧化物分子为非极性分子,其晶胞结构如右下图所示.原子序数为31的元素镓(Ga)与元素B形成的一种化合物是继以C单质为代表的第一代半导体材料和GaE为代表的第二代半导体材料之后,在近10年迅速发展起来的第三代新型半导体材料.湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com