
题目列表(包括答案和解析)
实验室配制有0.1mol/L的Na2CO3溶液,根据电离平衡和水解知识,回答下列有关问题:
⑴写出H2CO3的电离方程式为 ;
⑵Na2CO3溶液显碱性,原因是(用离子方程式表示)
;(2分)
⑶在该溶液中,c(Na+)、c(CO32-) 、c(H+)、c(HCO3-)、c(OH-)的大小关系为
;(2分)
⑷根据电荷守恒原理,该溶液中离子浓度关系有:
c(Na+)+c(H+)= ;(2分)
⑸根据物料守恒原理,该溶液中离子浓度关系有:
c(Na+)= 。(2分)
实验室配制有0.1mol/L的Na2CO3溶液,根据电离平衡和水解知识,回答下列有关问题:
⑴写出H2CO3的电离方程式为 ;
⑵Na2CO3溶液显碱性,原因是(用离子方程式表示)
;(2分)
⑶在该溶液中,c(Na+)、c(CO32-) 、c(H+)、c(HCO3-)、c(OH-)的大小关系为
;(2分)
⑷根据电荷守恒原理,该溶液中离子浓度关系有:
c(Na+)+c(H+)= ;(2分)
⑸根据物料守恒原理,该溶液中离子浓度关系有:
c(Na+)= 。(2分)
实验室配制有0.1mol/L的Na2CO3溶液,根据电离平衡和水解知识,回答下列有关问题:
⑴写出H2CO3的电离方程式为 ;
⑵Na2CO3溶液显碱性,原因是(用离子方程式表示)
;(2分)
⑶在该溶液中,c(Na+)、c(CO32-) 、c(H+)、c(HCO3-)、c(OH-)的大小关系为
;(2分)
⑷根据电荷守恒原理,该溶液中离子浓度关系有:
c(Na+)+c(H+)= ;(2分)
⑸根据物料守恒原理,该溶液中离子浓度关系有:
c(Na+)= 。(2分)
(2分)在K2Cr2O7+14HCI=2KCl+2CrCl3+3C12↑+7H2O反应中 (填化学符号,下同)是还原剂, 元素被还原。
已知A为常见的金属单质,根据图示的关系,回答下列问题.
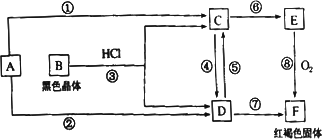
(1)(共4分)确定A、B、C、D的化学式,A为________,B为________,C为________,D为________,
(2)(共2分)在上述①~⑧的反应中属于非氧化还原反应的有________.
(3)(共4分)写出下列反应的化学(或离子)方程式:
D→C(写离子方程式)________;
E→F(写化学方程式)________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com