由于燃料电池汽车,尤其氢燃料电池汽车可以实现零污染排放,驱动系统几乎无噪音,且氢能取之不尽、用之不竭,燃料电池汽车成为近年来汽车企业关注的焦点.为了获得竞争优势,各国纷纷出台政策,加速推进燃料电池关键技术的研发.燃料电池的燃料有氢气、甲醇、汽油等.
(1)二氧化碳是地球温室效应的罪魁祸首,目前人们处理二氧化碳的方法之一是使其与氢气反应合成甲醇,甲醇是汽车燃料电池的重要燃料.已知氢气、甲醇燃烧的热化学方程式如下:
2H
2(g)+O
2 (g)=2H
2O (l)△H=-571.6kJ?mol
-1 ①
CH
3OH(l)+O
2(g)→CO
2(g)+2H
2O(l)△H=-726.0kJ?mol
-1 ②
写出二氧化碳与氢气合成甲醇液体的热化学方程式:
CO2 (g)+3H2 (g)=CH3OH(l)+H2O (l)△H=-131.4 kJ?mol-1
CO2 (g)+3H2 (g)=CH3OH(l)+H2O (l)△H=-131.4 kJ?mol-1
.
(2)有科技工作者利用稀土金属氧化物作为固体电解质制造出了甲醇一空气燃料电池.这种稀土金属氧化物在高温下能传导O
2-.
①电池正极发生的反应是
O2+4e-=2O2-
O2+4e-=2O2-
;
负极发生的反应是
CH2OH+4O2--8e-=CO2+2H2O
CH2OH+4O2--8e-=CO2+2H2O
.
②在稀土金属氧化物的固体电解质中,O
2-的移动方向是
从正极流向负极
从正极流向负极
.
③甲醇可以在内燃机中燃烧直接产生动力推动机动车运行,而科技工作者却要花费大量的精力研究甲醇燃料汽车.主要原因是:
燃料电池的能量转化率高
燃料电池的能量转化率高
.

 25℃、101kPa时甲醇质子交换膜燃料电池将甲醇蒸气转化为氢气的两种反应原理是:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0kJ?mol-1
25℃、101kPa时甲醇质子交换膜燃料电池将甲醇蒸气转化为氢气的两种反应原理是:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0kJ?mol-1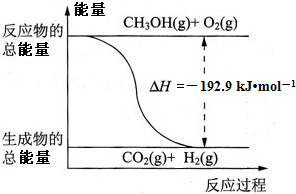 已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g),△H=+49.0kJ?mol-1
已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g),△H=+49.0kJ?mol-1