
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
œ÷”–“‘œ¬ŒÔ÷ £∫¢ŸKCIæßâ⁄ ≥—ŒÀÆ¢€“∫赃¥◊À·¢ÐI2¢ðBaSO4πÃâޒ·Ã«(C12H22O11 )¢þæ∆æ´(C2H5OH)¢ý»€»⁄µƒNaOH¢·K2O¢‚SO2°£«Îªÿ¥œ¬¡–Œ £∫
£®1£©“‘…œŒÔ÷ ÷–ƒÐµºµÁµƒ «_________________£®”√–Ú∫≈£©°£
£®2£©“‘…œŒÔ÷ Ù”⁄µÁΩ‚÷ µƒ «_________________£®”√–Ú∫≈£©°£
£®3£©“‘…œŒÔ÷ ÷– Ù”⁄∑«µÁΩ‚÷ µƒ «_________________£®”√–Ú∫≈£©°£
£®4£©¥”¢⁄»Ð“∫÷–µ√µΩ¬»ªØƒ∆πÃ㨔¶—°‘Òœ¬¡–◊∞÷√÷–µƒ______________£®ÃÓ¥˙±Ì◊∞÷√Õºµƒ◊÷ƒ∏£¨œ¬Õ¨£©£ª∑÷¿Î¢Ð”΢þµƒªÏ∫œ“∫£¨”¶—°‘Òœ¬¡–◊∞÷√÷–µƒ________________°£
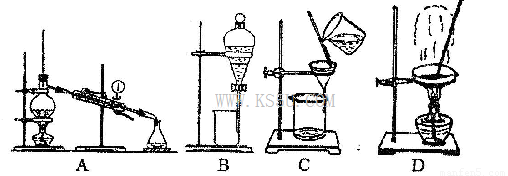
£®5£©«Î–¥≥ˆ¢€∫Õ¢ý÷–¡Ω÷÷ŒÔ÷ µƒ»Ð“∫ªÏ∫œ∫Û∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω£∫________________________________________________________________________£Æ
£®6£©‘⁄±Í◊º◊¥øˆœ¬£¨__________L¢‚”Î34£Æ 2g¢Þ÷–∫¨”–œýÕ¨µƒ—ı‘≠◊” ˝°£
œ÷”–“‘œ¬ŒÔ÷ £∫¢ŸKCIæßâ⁄ ≥—ŒÀÆ¢€“∫赃¥◊À·¢ÐI2¢ðBaSO4πÃâޒ·Ã«(C12H22O11 )¢þæ∆æ´(C2H5OH)¢ý»€»⁄µƒNaOH¢·K2O¢‚SO2°£«Îªÿ¥œ¬¡–Œ £∫
£®1£©“‘…œŒÔ÷ ÷–ƒÐµºµÁµƒ «_________________£®”√–Ú∫≈£©°£
£®2£©“‘…œŒÔ÷ Ù”⁄µÁΩ‚÷ µƒ «_________________£®”√–Ú∫≈£©°£
£®3£©“‘…œŒÔ÷ ÷– Ù”⁄∑«µÁΩ‚÷ µƒ «_________________£®”√–Ú∫≈£©°£
£®4£©¥”¢⁄»Ð“∫÷–µ√µΩ¬»ªØƒ∆πÃ㨔¶—°‘Òœ¬¡–◊∞÷√÷–µƒ______________£®ÃÓ¥˙±Ì◊∞÷√Õºµƒ◊÷ƒ∏£¨œ¬Õ¨£©£ª∑÷¿Î¢Ð”΢þµƒªÏ∫œ“∫£¨”¶—°‘Òœ¬¡–◊∞÷√÷–µƒ________________°£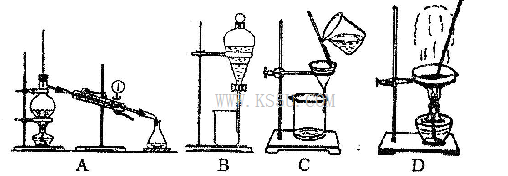
£®5£©«Î–¥≥ˆ¢€∫Õ¢ý÷–¡Ω÷÷ŒÔ÷ µƒ»Ð“∫ªÏ∫œ∫Û∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω£∫________________________________________________________________________£Æ
£®6£©‘⁄±Í◊º◊¥øˆœ¬£¨__________L¢‚”Î34£Æ 2g¢Þ÷–∫¨”–œýÕ¨µƒ—ı‘≠◊” ˝°£
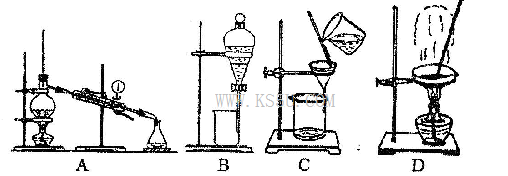
ªÿ¥“‘œ¬πÿ”⁄µ⁄»˝÷Ð∆⁄‘™Àÿº∞∆‰ªØ∫œŒÔµƒŒ °£
£®1£©œ¬¡–ƒÐ”√”⁄≈–∂œ—ı∫Õ∑˙∑«Ω Ù–‘«ø»ıµƒ « £®—°ÃÓ±ý∫≈£©°£
A£Æ∆¯Ã¨«‚ªØŒÔµƒŒ»∂®–‘ B£Æ◊Ó∏þº€—ıªØŒÔ∂‘”¶Àƪ،ԵƒÀ·–‘
C£Æµ•÷ ”Ϋ‚∆¯∑¥”¶µƒƒ—“◊ D£Æµ•÷ ”ÎÕ¨≈®∂»À·∑¢…˙∑¥”¶µƒøϬ˝
£®2£©Be∫ÕAlæþ”–œýÀ∆µƒªØ—ß–‘÷ £¨–¥≥ˆBeCl2ÀÆΩ‚∑¥”¶µƒªØ—ß∑Ω≥à Ω
£®3£©≥£Œ¬œ¬£¨≤ªƒÐ”ά¡µ•÷ ∑¢…˙∑¥”¶µƒ «_________£®ÃÓ–Ú∫≈£©
A£ÆCuSO4»Ð“∫ B£ÆFe2O3 C£Æ≈®¡ÚÀ· D£ÆNaOH E£ÆNa2CO3πÃÃÂ
£®4£©œýÕ¨—π«øœ¬£¨≤ø∑÷‘™Àÿ∑˙ªØŒÔµƒ»€µ„º˚œ¬±Ì£∫
| ∑˙ªØŒÔ | NaF | MgF2 | SiF4 |
| »€µ„/°Ê | 1266 | 1534 | 183 |
 2Cl2+2H2O£¨ø… µœ÷¬»µƒ—≠ª∑¿˚”√°£
2Cl2+2H2O£¨ø… µœ÷¬»µƒ—≠ª∑¿˚”√°£ P
P Q
Q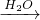 M+P
M+Pπ˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com