
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)

¢Ÿ…˺∆º◊◊∞÷√µƒƒøµƒ «_________________°£º◊◊∞÷√__________£®ÃÓ°∞ƒÐ°±ªÚ°∞≤ªƒÐ°±£©”√““◊∞÷√¿¥¥˙ÃÊ°£
¢⁄◊∞÷√““÷– ¢”–µƒ“∫à«__________£¨∏√◊∞÷√ø…ø¥◊˜ «“ª∏ˆ___________£®ÃÓƒ≥“«∆˜√˚≥∆£©°£
£®2£©‘⁄µ™µƒªØ∫œŒÔ÷–£¨”–“ª¿ý—ŒΩ–—«œıÀ·—Œ£¨»Á—«œıÀ·ƒ∆£®NaNO2£©µ»°£NaNO2 «“ª÷÷«±‘⁄µƒ÷¬∞©ŒÔ÷ £¨π˝¡øªÚ≥§∆⁄ π”√ª·∂‘»À≤˙…˙Œ£∫¶°£”…”⁄—«œıÀ·ƒ∆”–œÃŒ∂£¨Õ‚π€”ÎNaClœýÀ∆£¨‘¯∂ý¥Œ∑¢…˙π˝±ªŒÛµ± ≥—Œ π”√µƒ ¬º˛°£“—÷™£∫HNO2 «“ª÷÷»ıÀ·£¨≤ªŒ»∂®£¨“◊∑÷Ω‚…˙≥…NO∫ÕNO2£ªÀ¸ƒÐ±ª≥£º˚µƒ«ø—ıªØº¡—ıªØ£ª‘⁄À·–‘»Ð“∫÷–À¸“≤ «“ª÷÷—ıªØº¡£¨»ÁƒÐ∞—I-—ıªØ≥…I2;AgNO2 «“ª÷÷ƒ—»Ð”⁄ÀÆ“◊»Ð”⁄À·µƒªØ∫œŒÔ°£ ‘ªÿ¥œ¬¡–Œ £∫
¢Ÿ»ÀÃÂ’˝≥£µƒ—™∫ϵ∞∞◊÷–”¶∫¨Fe2+°£»ÙŒÛ ≥—«œıÀ·—Œ£®»ÁNaNO2£©£¨‘Úµº÷¬—™∫ϵ∞∞◊÷–Fe2+◊™ªØŒ™Fe3+∂¯÷–∂棨∑˛”√Œ¨…˙ÀÿCø…Ω‚∂æ°£œ¬¡–– ˆ≤ª’˝»∑µƒ «_____________°£
A.—«œıÀ·—Œ «ªπ‘≠º¡ B.Œ¨…˙ÀÿC «ªπ‘≠º¡
C.Œ¨…˙ÀÿCΩ´Fe3+ªπ‘≠Œ™Fe2+ D.—«œıÀ·—Œ±ªªπ‘≠
¢⁄œ¬¡–Àµ∑®÷–£¨ƒÐ”√¿¥«¯±NaNO2∫ÕNaClµƒ «______________°£
A.≤‚∂®’‚¡Ω÷÷»Ð“∫µƒpH
B.”√AgNO3∫ÕHNO3¡Ω÷÷ ‘º¡¿¥«¯±
C.‘⁄À·–‘Ãıº˛œ¬º”»ÎKIµÌ∑€ ‘“∫¿¥«¯±
¢€∞—–¬÷∆¬»∆¯Õ®»ÎµΩNaNO2»Ð“∫÷–£¨¬»ÀÆÕ …´£¨…˙≥…NaNO3∫ÕHCl£¨«Î–¥≥ˆ¥À∑¥”¶µƒ¿Î◊”∑Ω≥à Ω______________°£
¢ÐŒ™¡À≤‚∂®ƒ≥—˘∆∑÷–NaNO2µƒ∫¨¡ø£¨ø…“‘ π”√±Í◊º?KMnO4?»Ð“∫Ω¯––µŒ∂®£¨ ‘ªÿ¥£∫KMnO4»Ð“∫‘⁄µŒ∂®π˝≥Ã÷–◊˜____________£®ÃÓ°∞—ıªØº¡°±ªÚ°∞ªπ‘≠º¡°±£©£¨∏√µŒ∂®π˝≥Ã_____________£®ÃÓ°∞“™°±ªÚ°∞≤ª“™°±£©¡Ìº”÷∏ 溡°£
¢ð“—÷™HNO2µƒÀ·–‘±»¥◊À·¬‘«ø£¨ƒ≥Õ¨—ß‘⁄º“÷–Ω¯––º¯±NaNO2”ÎNaClµƒ µ—È£¨µ´À˚º“÷–÷ª”–≈®¥◊À·£¨«ÎŒ ∏√ µ—ȃÐ∑Ò≥…π¶£ø____________£®ÃÓ°∞ƒÐ°±ªÚ°∞≤ªƒÐ°±£©£¨«ÎÀµ√˜¿Ì”…_______
_____________________________________________________________________°£
| ||
| ¥þªØº¡ |
| NaOH |
| °˜ |
| NaOH |
| °˜ |
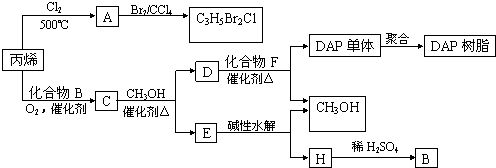
| NaOH»Ð“∫ | “¯∞±»Ð“∫ | –¬÷∆Cu£®OH£©2 | Ω Ùƒ∆ | |
| X | ÷–∫Õ∑¥”¶ | ŒÞœ÷œÛ | »Ð Ω‚ | ≤˙…˙«‚∆¯ |
| Y | ŒÞœ÷œÛ | ”–“¯æµ | º”»»∫Û”–∫Ï…´≥¡µÌ | ≤˙…˙«‚∆¯ |
| Z | ÀÆΩ‚∑¥”¶ | ”–“¯æµ | º”»»∫Û”–∫Ï…´≥¡µÌ | ŒÞœ÷œÛ |
| W | ÀÆΩ‚∑¥”¶ | ŒÞœ÷œÛ | ŒÞœ÷œÛ | ŒÞœ÷œÛ |


∞¢Àπ∆•¡÷£®aspirin£©µƒ”––ß≥…∑÷ «““ı£ÀÆ—ÓÀ·£¨À¸ «19 ¿ºÕƒ©∫œ≥…≥…𶵃£¨◊˜Œ™“ª∏ˆ”––ßµƒΩ‚»»÷πÕ¥°¢÷Œ¡∆∏–√∞µƒ“©ŒÔ£¨÷¡ΩÒ»‘π„∑∫ π”√£¨”–πÿ±®µ¿±Ì√˜£¨»À√«’˝‘⁄∑¢œ÷À¸µƒƒ≥–©–¬π¶ƒÐ°£∞¢Àπ∆•¡÷ «”…ÀÆ—ÓÀ·£®¡⁄Ù«ª˘±Ωº◊À·£©”Γ“À·Ù˚Ω¯––ı•ªØ∑¥”¶∂¯µ√µƒ°£
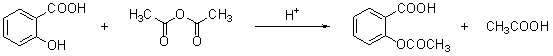
ÀÆ—ÓÀ· ““À·Ù˚ ““ı£ÀÆ—ÓÀ·
£®1£©““ı£ÀÆ—ÓÀ·µƒ∫¨—ıπŸƒÐÕ≈∑÷± «_____________∫Õı•ª˘°£
£®2£©““ı£ÀÆ—ÓÀ·ƒÐ‘⁄œ°À·∫ÕNaOH»Ð“∫÷–ÀÆΩ‚°£–¥≥ˆ““ı£ÀÆ—ÓÀ·”Îœ°À·»Ð“∫π≤»»µƒªØ—ß∑Ω≥Ã Ω£∫___________°£
£®3£©–¥≥ˆÕ¨ ±∑˚∫œœ¬¡–Àƒ∏ˆ“™«ÛµƒÀÆ—ÓÀ·µƒÕ¨∑÷“Ïππã∫°°°°°°°°°°°°°£
¢Ÿ∫¨”–±Ωª∑£ª
¢⁄ƒÐ∑¢…˙“¯æµ∑¥”¶£¨≤ªƒÐ∑¢…˙ÀÆΩ‚∑¥”¶£ª
¢€‘⁄œ°NaOH»Ð“∫÷–£¨1 mol∏√Õ¨∑÷“ÏππÃДÎ2 mol NaOH∑¢…˙∑¥”¶£ª
¢Ð÷ªƒÐ…˙≥…¡Ω÷÷“ª¬»¥˙≤˙…˙°£
£®4£©“—÷™∑”Ù«ª˘”ˆFeC13»Ð“∫œ‘◊œ…´£¨µ´œ‘…´∑¥”¶“™‘⁄÷––‘ªÚ»ıÀ·–‘»Ð“∫Ω¯––°£œ÷“™«Û”√“—”–µƒ÷™ ∂ºÏ—È≥ˆ““ı£ÀÆ—ÓÀ·∑÷◊”÷–¥Ê‘⁄ı•ª˘°£”–»À…˺∆¡À»Áœ¬µƒ µ—È∑Ω∞∏£∫
»°“ª÷ßΩý檵ƒ ‘πУ¨œÚ∆‰÷–º”»Î2mL∞¢Àπ∆•¡÷«Â“∫£¨»ª∫Û‘ŸµŒ»Î2 µŒœ°¡ÚÀ·£¨Ω´»Ð“∫‘⁄æ∆æ´µ∆…œº”»»∆¨øÃ∫Û£¨µŒ»Î2µŒFeC13»Ð“∫£¨’Òµ¥£¨ŒÞ√˜œ‘œ÷œÛ£ª‘ŸœÚ∆‰÷–÷µŒº”»ÎNa2CO3»Ð“∫£¨’Òµ¥£¨≥ˆœ÷¡À◊œ…´°£ƒ„»œŒ™÷µŒº”»ÎNa2CO3»Ð“∫µƒƒøµƒ «_____________°£¥”¥À µ—ȃ„µ√µΩµƒ∆Ù æ”–_____________°£
£®5£©Œ™≤‚∂®∞¢Àπ∆•¡÷÷–”––ß≥…∑÷µƒ∫¨¡ø£¨≥∆»°—˘∆∑0.250 0 g £¨◊º»∑º”»Î≈®∂»Œ™0.1015 mol?L- NaOH»Ð“∫50.00 mL£¨÷Û∑–60min°£¿‰»¥∫Û”√≈®∂»Œ™0.1015 mol?L- µƒHC1»Ð“∫∑µµŒπ˝¡øµƒNaOH£¨œ˚∫ƒHC1»Ð“∫º«¬º»Áœ¬£∫
| ˝æ𠥌 ˝ | 1 | 2 | 3 |
| ≥ı º∂¡ ˝ | 2.00 | 12.50 | 5.20 |
| ◊Ó∫Û∂¡ ˝ | 27.10 | 37.40 | 33.20 |
‘Ú∏√≤˙∆∑÷–““ı£ÀÆ—ÓÀ·µƒ∫¨¡øŒ™(““ı£ÀÆ—ÓÀ·µƒƒ¶∂˚÷ ¡ø «180.16 g?mol- °££®÷ª“™«Û¡– Ω±Ì æ£¨≤ªº∆À„≥ˆ◊Ó∫ÛΩ·π˚£©____________°£
(1)÷–—ßªØ—ß µ—È÷–µƒ÷–∫Õ»»µƒ≤‚∂®À˘–˵ƒ≤£¡ß“«∆˜≥˝…’±≠∫ÕŒ¬∂»º∆Õ‚ªπ”–°°°°°°°°°£?
(2)∏√ µ—È≥£”√0.50 mol°§L-1HCl∫Õ0.55 mol°§L-1?µƒNaOH»Ð“∫∏˜50 mLΩ¯––∑¥”¶°£ µ—È÷–£¨ πNaOH»Ð“∫…‘π˝¡øµƒ÷˜“™‘≠“Ú «°° °£?
(3)»Ù…œ ˆHCl°¢NaOH»Ð“∫µƒ√Ð∂»∂ºΩ¸À∆Œ™1 g°§cm-3£¨»Ù∑¥”¶«∞∫ÛµƒŒ¬∂»∑÷±Œ™t1°Ê°¢?t2°Ê,÷–∫Õ∫Û…˙≥…µƒ»Ð“∫µƒ±»»»»ðc =4.18 J/(g°§°Ê)£¨‘Ú∏√÷–∫Õ∑¥”¶∑≈≥ˆ»»¡øŒ™°°°°°°kJ(ÃÓ±Ì¥Ô Ω)£¨∆‰÷–∫Õ»»¶§H?°°°°°°°°kJ°§mol-1(ÃÓ±Ì¥Ô Ω)°£?
¢Ú.∏˘æðø∆—ß µ—ÈÕ≥º∆£¨œ„—×ÌÌ÷–”–1 000∂ý÷÷ªØ∫œŒÔ°£∆‰÷–÷¡…Ÿ”–300÷÷ªØ∫œŒÔ‘⁄≤ªÕ¨≥Ã∂»…œ”–∂棨»Á“ª—ıªØú°¢ƒ·π≈∂°°¢»©¿ýµ»°£ƒ≥ªØ—ßøŒÕ‚ªÓ∂Ø–°◊ȅ˺∆ µ—ȺϗȜ„—×ÌÌ÷–¥Ê‘⁄“ª—ıªØú°¢ƒ·π≈∂°°¢»©¿ýµ»”–∂æŒÔ÷ °£?

»Á…œÕº£¨D ‘πеƒ÷ßπДÎ≥È∆¯◊∞÷√œý¡¨£¨¥”D ‘πеƒ÷ßπÐ¥¶≥È∆¯£¨ø… πA…œ»º◊≈µƒœ„—õƒ—Ì̓¿¥ŒÕ®π˝A°¢B°¢C°¢DÀƒ∏ˆ◊∞÷√£¨«“√ø∏ˆ◊∞÷√÷ªƒÐŒ¸ ’“ª÷÷ŒÔ÷ (A¥¶œ„—Ãø…¡¨–¯»º…’)°£

(1)ƒ·π≈∂°µƒΩ·ππ»Á…œ£¨‘⁄ƒ·π≈∂°Ω·ππ Ω÷–¡˘‘™ª∑…œµƒ“ª¬»»°¥˙ŒÔ”–°° ÷÷°£?
(2)»Ù”√B◊∞÷√ºÏ—È»©¿ýŒÔ÷ £¨‘Ú ‘πÐB÷– ¢◊∞µƒ ‘º¡ «°°°°°°°°°°°£?
(3)“—÷™£∫‘⁄—™“∫÷–¥Ê‘⁄œ¬ ˆ∆Ω∫‚£∫?
—™∫ϵ∞∞◊°™O2+CO![]() —™∫ϵ∞∞◊°™CO+O2?
—™∫ϵ∞∞◊°™CO+O2?
(—™∫Ï…´) (œ ∫Ï…´)?
»Ù”√D◊∞÷√ºÏ—ÈCOµƒ¥Ê‘⁄£¨‘Úø…≤…”√D ‘πÐ÷–º”»Î5 mL–¬œ ∂،ԗ™£¨∆‰ µ—Èœ÷œÛŒ™°°°°°°°°°°°°°°°°°£∏√∆¯ÃÂ∂‘»ÀÔ–∫¶£¨µ±∑¢…˙÷–∂æ ±£¨ø…≤…»°µƒ¡Ω÷÷¥Î © «¢Ÿ°°°°°°°°°°£ª¢⁄°°°°°°°°°°°£“¿æ𵃑≠¿Ì «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£
(15∑÷)±æÂŒ™—°◊ˆÃ‚£¨∞¸¿®A°¢B¡Ω°£—°—ß°∂ªØ—ߔ΅˙ªÓ°∑ƒ£øȵƒøº…˙¥A£¨—°—ß°∂”–ª˙ªØ—ߪ˘¥°°∑ƒ£øȵƒøº…˙¥B£¨√øŒªøº…˙÷ªø…—°◊ˆ1°£»Ù¡ΩÂ∂º◊˜¥£¨‘Ú“‘Aº∆∑÷°£
A£Æ°∂ªØ—ߔ΅˙ªÓ°∑
¢≈(3∑÷)ÀÊ◊≈𧓵ªØ°¢≥«’ڪصƒøÏÀŸ∑¢’π£¨Œ“√«À˘…˙¥Êµƒª∑æ≥“≤√Ê¡Ÿ‘Ω¿¥‘Ω—œæ˛µƒŒ€»æŒ £¨»ÁÀ·”͵ƒ–Œ≥…°¢∆˚≥µŒ≤∆¯Œ€»æ°¢π§“µ∑œ∆¯Œ€»æ°¢¥Û¡ø…˙ªÓ¿¨ª¯µƒ≤˙…˙µ»°£
¢Ÿœ¬¡–¥Î ©≤ªƒÐπª∏ƒ…∆ª∑æ≥÷ ¡øµƒ « (ÃÓ◊÷ƒ∏)°£
a£Æ∂‘À˘”–¿¨ª¯Õ®π˝¬∂ÃÏ∑Ÿ…’µƒ∑Ω ΩΩ¯––¥¶¿Ì
b£Æ∏¯∆˚≥µ≈≈∆¯πк”◊∞Œ≤∆¯¥þªØ檪Ø◊∞÷√“‘ºı…ŸŒ≤∆¯Œ€»æ
c£Æ‘⁄√∫Ãø÷–Ã̺”…˙ ت““‘ºı…ŸÀ·”͵ƒ∑¢…˙
¢⁄≥« –ø’∆¯÷ ¡øºý≤‚÷–£¨≤ª–Ë“™ºý≤‚µƒ÷∏±Íµƒ « (ÃÓ◊÷ƒ∏)°£
a£ÆSO2≈®∂» b£ÆNOx≈®∂» c£Æø…Œ¸»Îø≈¡£ŒÔµƒ∫¨¡ø d£ÆCO2≈®∂»
¢€œ÷¥˙»À“—æ≠Ω¯»Î“‘°∞ “ƒ⁄Œ€»æ°±Œ™±Í÷浃µ⁄»˝∏ˆŒ€»æΩ◊∂Œ£¨“‘œ¬≤ª Ù”⁄ “ƒ⁄Œ€»æŒÔµƒ «
(ÃÓ◊÷ƒ∏)°£
a£Æ≈΂ø ±≤˙…˙µƒ”Õ—Ã b£Æ Ø≤ƒª∫¬˝ Õ∑≈µƒ∑≈…‰–‘∆¯ÃÂ
c£Æ∏˜÷÷∞Â≤ƒ÷–’≥∫œº¡ Õ∑≈µƒº◊»©µ» d£ÆÃÏ»ª∆¯»º…’≤˙…˙µƒCO2∫ÕÀÆ
¢∆(6∑÷)ªØ—ߔΖ¬≤ƒ¡œø™∑¢√Ы–πÿ¡™£¨ªØ—ß «»À¿ýΩ¯≤Ωµƒπÿº¸°£

¢ŸΩ¸»’£¨°∂÷–π˙∫Ωø’±®°∑Õ∏¬∂¡À“ªÃı÷ÿ¥Ûœ˚œ¢£¨÷–π˙‘⁄œ»Ω¯∏þŒ¬∫œΩ¡Ï”Ú≤ª∂œªÒµ√÷ÿ¥Û≥…π˚°£ø…“‘Àµ£¨√ª”–∏þŒ¬∫œΩ£¨æÕ√ª”–ΩÒÃÏœ»Ω¯µƒ∫Ωø’∑¢∂ت˙°£œ¬¡–ŒÔ÷ ÷–≤ª Ù”⁄∫œΩµƒ « (ÃÓ◊÷ƒ∏)°£
a£Æ”≤¬¡ b£Æ≤£¡ß∏÷ c£Æ≤ª–‚∏÷ d£Æª∆Õ≠
¢⁄–¬–Õ”–ª˙≤£¡ßÕ∏π‚–‘∫√£¨÷ «·£¨ƒÕÀ·°¢ºÓ£¨“◊”⁄º”π§≥…–Õ£¨«ø∂»∏þ£¨∞≤»´–‘∫√°£”–ª˙≤£¡ß Ù”⁄ (ÃÓ°∞∫œ≥…œÀŒ¨°±°¢°∞∫œ≥…œΩ∫°±ªÚ°∞ÀСœ°±)≤ƒ¡œ°£ª∑±£–Õ怓“œ©ÀСœ¥¸ø…“‘”√”⁄ ≥∆∑∞¸◊∞£¨∫œ≥…∏√æ€∫œŒÔµƒ∑¥”¶ø…±Ì 挙 °£
¢€ÀÊ◊≈µÁق𧓵µƒ∑¢’𣨬¡÷∆∆∑“—æ≠±ª»À¿ýπ„∑∫ π”√£¨µ´ «≥£Œ¬œ¬≤ªø…“‘”√¬¡÷∆»ð∆˜ ¢◊∞µƒ « (ÃÓ◊÷ƒ∏)°£
a£Æ≈®«‚—ıªØƒ∆»Ð“∫ b£Æ≈®¡ÚÀ· c£Æ≈®œıÀ· d£Æ∆°æ∆
‘⁄ “Õ‚£¨≤ªƒÐΩ´Õ≠÷ µÁœþ∫Õ¬¡÷ µÁœþ÷±Ω”œý¡¨Ω”£¨∑Ò‘Úª·“Ú∑¢…˙ ∏Ø ¥∂¯–Œ≥…∞≤»´“˛ªº°£
¢«(6∑÷)∫œ¿Ì…≈ ≥£¨±£≥÷”™—¯æ˘∫‚£¨∫œ¿Ì π”√“©ŒÔ ««ý…ŸƒÍ—ß…˙Ω°øµ≥…≥§µƒ÷ÿ“™±£÷§°£
¢ŸŒ¨…˙ÀÿCƒÐ‘ˆ«ø»ÀÃÂ∂‘º≤≤°µƒµ÷øπƒÐ¡¶£¨¥ŸΩ¯»ÀÃÂ…˙≥§∑¢”˝°£‘⁄¬»ªØÃ˙»Ð“∫÷–º”»ÎŒ¨…˙ÀÿC»Ð“∫∫Û£¨»Ð“∫”…ª∆…´◊™±‰Œ™«≥¬Ã…´£¨Àµ√˜Œ¨…˙ÀÿCæþ”– –‘°£
¢⁄ £®ÃÓ◊÷ƒ∏£©æþ”–÷πø»∆Ω¥≠◊˜”√£¨ø…”√”⁄÷Œ¡∆÷ß∆¯πÐœ¯¥≠°¢±«’≥ƒ§≥‰—™“˝∆µƒ±«»˚µ»°£
a£Æ¬Èª∆ºÓ b£Æ∞¢Àæ∆•¡÷ c£ÆøπÀ·“© d£Æ«ý√πÀÿ
¢€»À√«√øÃÏ…„»°µƒ»»ƒÐ÷–¥Û‘º”–75%¿¥◊‘ë¿ý£¨µÌ∑€ «“ª÷÷÷ÿ“™µƒ∂ý루À¸‘⁄»ÀÃ⁄ÀÆΩ‚µƒ◊Ó÷’≤˙ŒÔ « £®ÃÓ∑÷◊” Ω£©°£µ‚‘™Àÿ «»Àñÿ–˵ƒŒ¢¡ø‘™Àÿ÷Æ“ª£¨”–°∞÷«¡¶‘™Àÿ°±÷Æ≥∆£¨ƒø«∞£¨Œ“π˙Õ®π˝‘⁄ ≥—Œ÷–º”»Î £®ÃÓªØ—ß Ω£©¥”∂¯¥ÔµΩ≤𵂵ƒ–ßπ˚°£…˙ŒÔ÷∆“©÷–Õ˘Õ˘…ʺ∞µΩªÓ–‘µ∞∞◊÷ µƒÃ·¥ø£¨ø…“‘≤…”√µƒ“ª÷÷∑Ω∑® « £®ÃÓ°∞π˝¬À°±°¢°∞∏þŒ¬’Ù¡Û°±ªÚ°∞—ŒŒˆ°±£©°£µÌ∑€°¢œÀŒ¨Àÿ°¢”Õ÷¨°¢µ∞∞◊÷ ÷–≤ª Ù”⁄ÃÏ»ª∏þ∑÷◊”µƒ « °£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com