
题目列表(包括答案和解析)
[ ]
下列说法正确的是 ( )
A.25℃时,任何稀溶液中由水电离出的c(H+)和c(OH-)的乘积都为1×10-14mol2·L-2
B.氯气溶于水达到平衡后,若其他条件不变,加入少量水,水的电离平衡向逆向移动
C.电解法精炼铜,当阴极质量增加32 g时,有6.02×1023个电子转移
D.含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为6.02×1022
下列说法正确的是
A.AgCl水溶液的导电性很弱,所以AgCl为弱电解质
B.溶度积反映了难溶电解质在水中的溶解能力,所以溶度积大的化合物溶解能力肯定大
C.将难溶电解质放入纯水中,溶解达平衡时,电解质离子的浓度的乘积就是该物质的溶度积
D.一定温度下,向含有AgCl固体的溶液中加入适量的水使AgCl溶解又达到平衡时,AgCl的溶度积不变,其溶解度也不变
难溶物质在水中达到溶解平衡的溶度积常数与水的电离平衡常数相似。则关于BaSO4溶解平衡:BaSO4(s)![]() Ba2+(aq)+SO42-(aq)的下列说法正确的是( )
Ba2+(aq)+SO42-(aq)的下列说法正确的是( )
A.溶液的温度升高,BaSO4的溶度积常数不变
B.在Na2SO4溶液中,BaSO4的溶解度不变
C.在BaCl2溶液中,BaSO4的溶度积常数变小
D.精制NaCl时,在溶液中加入稍过量的BaCl2溶液是为了更好地除去SO42-等离子
难溶物质在水中达到溶解平衡的溶度积常数与水的电离平衡常数相似。则关于BaSO4溶解平衡:BaSO4(s)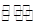 Ba2+(aq)+SO42-(aq)的下列说法正确的是(
)
Ba2+(aq)+SO42-(aq)的下列说法正确的是(
)
A.溶液的温度升高,BaSO4的溶度积常数不变
B.在Na2SO4溶液中,BaSO4的溶解度不变
C.在BaCl2溶液中,BaSO4的溶度积常数变小
D.精制NaCl时,在溶液中加入稍过量的BaCl2溶液是为了更好地除去SO42-等离子
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com