
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
“—÷™¥◊À·∫Õ—ŒÀ· «»’≥£…˙ªÓ÷–º´Œ™≥£º˚µƒÀ·£¨‘Ğ“ª∂®Ãº˛œ¬,CH3COOH»İ“∫÷–¥Ê‘еÁ¿Î∆Ω∫‚£∫CH3COOH ![]() CH3COO-+H+ ¶§H>0°£
CH3COO-+H+ ¶§H>0°£
£®1£©25 °Ê ±£¨≈®∂»æ˘Œ™0.1mol/Lµƒ—ŒÀ·∫Õ¥◊À·»İ“∫£¨œ¬¡–Àµ∑®’˝»∑µƒ « £ª
¢Ÿ¡Ω»İ“∫µƒpHœ‡Õ¨
¢Ğ¡Ω»İ“∫µƒµºµÁƒİ¡¶œ‡Õ¨
¢ğ”…ÀƵÁ¿Î≥ˆµƒc(OH-)œ‡Õ¨
¢İ÷–∫Õµ»ŒÔ÷ µƒ¡øµƒNaOH»İ“∫£¨œ˚∫ƒ¡Ω»İ“∫µƒÃª˝œ‡Õ¨
£®2£©25 °Ê ±£¨‘Ğ pH =5µƒœ°¥◊À·»İ“∫÷–£¨c(CH3COO-)= (ÃÓ ˝◊÷±Ì¥Ô Ω)£ª
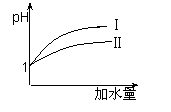 £®3£©25 °Ê ±£¨œÚpHæ˘Œ™1µƒ—ŒÀ·∫Õ¥◊À·»İ“∫÷–∑÷±º”ÀÆ£¨Àʺ”ÀÆ
£®3£©25 °Ê ±£¨œÚpHæ˘Œ™1µƒ—ŒÀ·∫Õ¥◊À·»İ“∫÷–∑÷±º”ÀÆ£¨Àʺ”ÀÆ
¡øµƒ‘ˆ∂‡£¨¡Ω»İ“∫pHµƒ±‰ªØ»ÁÕºÀ˘ 棨‘Ú∑˚∫œ—ŒÀ·pH±‰ªØ
µƒ«˙œş « £ª
£®4£©25 °Ê ±£¨œÚê˝Œ™Va mLpH=3µƒ¥◊À·»İ“∫÷–µŒº”pH=11µƒ
NaOH»İ“∫Vb mL÷¡»İ“∫«°∫√≥ ÷––‘£¨‘ÚVa”εƒVbπÿœµ «
Va Vb£®ÃÓ°∞£æ°±°¢°∞£º°±ªÚ°∞£Ω°±£©°£
£®5£©25 °Ê ±£¨»ÙœÚ∞±ÀÆ÷–º”»Îœ°—ŒÀ·÷¡»İ“∫µƒpH£Ω7£¨¥À ±[NH4£´]£Ωa mol/L£¨
‘Ú[Cl£≠]£Ω________°£
µ ©“‘º…Ÿƒİ‘¥¿À∑—∫ÕΩµµÕ∑œ∆¯≈≈∑≈Œ™ª˘±æƒĞ»ıµƒΩЃݺ≈≈’˛≤ş£¨ «”¶∂‘»´«Ú∆¯∫ÚŒ °¢Ω®…Ë◊ ‘¥ΩĞ‘º–Õ°¢ª∑æ≥”—∫√–Õ…Áª·µƒ±ÿ»ª—°‘Ò°£ªØπ§––“µµƒ∑¢’π±ÿ–Î∑˚∫œπ˙º“ΩЃݺ≈≈µƒ◊İÓ™«Û£¨“¿øø¿Ì¬ğ÷™ ∂◊ˆª˘¥°°£ ‘‘À”√À˘—ß÷™ ∂£¨Ω‚戜¬¡–Œ £∫
£®1£©“—÷™ƒ≥∑¥”¶µƒ∆Ω∫‚±Ì¥Ô ΩŒ™£∫ À¸À˘∂‘”¶µƒªØ—ß∑¥”¶Œ™£∫_____________________________
À¸À˘∂‘”¶µƒªØ—ß∑¥”¶Œ™£∫_____________________________
£®2£©¿˚”√ÀÆ√∫∆¯∫œ≥…∂˛º◊√—µƒ»˝≤Ω∑¥”¶»Áœ¬£∫
¢Ÿ2H2£®g£©+CO£®g£©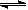 CH3OH£®g£©£ª¶§H=£≠90.8 kJ/mol
CH3OH£®g£©£ª¶§H=£≠90.8 kJ/mol
¢Ğ2CH3OH£®g£©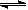 CH3OCH3£®g£©+H2O£®g£©£ª¶§H=£≠23.5 kJ/mol
CH3OCH3£®g£©+H2O£®g£©£ª¶§H=£≠23.5 kJ/mol
¢ğCO£®g£©+ H2O£®g£©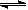 CO2£®g£©+H2£®g£©£ª¶§H=£≠41.3 kJ/mol
CO2£®g£©+H2£®g£©£ª¶§H=£≠41.3 kJ/mol
◊İ∑¥”¶£∫3H2£®g£©+3CO£®g£©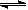 CH3OCH3£®g£©+CO2£®g£©µƒ¶§H=__________ £¨
CH3OCH3£®g£©+CO2£®g£©µƒ¶§H=__________ £¨
∂˛º◊√—£®CH3OCH3£©÷±Ω”◊˜»º¡œµÁ≥ÿæş”–∆Ù∂ØøÏ£¨–߬ ∏şµ»”≈µ„£¨»ÙµÁΩ‚÷ Œ™À·–‘£¨∏√µÁ≥ÿµƒ∏∫º´∑¥”¶Œ™_____________________________°£
£®3£©√∫ªØπ§Õ®≥£Õ®π˝—–æø≤ªÕ¨Œ¬∂»œ¬∆Ω∫‚≥£ ˝“‘Ω‚æˆ∏˜÷÷ µº Œ °£“—÷™µ»Ãª˝µƒ“ª—ªØú∫ÕÀÆ’Ù∆¯Ω¯»Î∑¥”¶∆˜ ±£¨ª·∑¢…˙»Áœ¬∑¥”¶£∫CO£®g£©+H2O£®g£© ? H2£®g£©+CO2£®g£©£¨∏√∑¥”¶∆Ω∫‚≥£ ˝ÀÊŒ¬∂»µƒ±‰ªØ»Áœ¬±ÌÀ˘ æ£∫
? H2£®g£©+CO2£®g£©£¨∏√∑¥”¶∆Ω∫‚≥£ ˝ÀÊŒ¬∂»µƒ±‰ªØ»Áœ¬±ÌÀ˘ æ£∫
Œ¬∂»/°Ê | 400 | 500 | 800 |
∆Ω∫‚≥£ ˝K | 9.94 | 9 | 1 |
∏√∑¥”¶µƒ’˝∑¥”¶∑ΩœÚ «_________∑¥”¶£®ÃÓ°∞Œ¸»»°±ªÚ°∞∑≈»»°±£©£¨»Ù‘Ğ500°Ê ±Ω¯––£¨…Ë∆ º ±CO∫ÕH2Oµƒ∆ º≈®∂»æ˘Œ™0.020mol/L£¨‘Ğ∏√ú˛œ¬£¨COµƒ∆Ω∫‚◊™ªØ¬ Œ™£∫________°£
£®4£©¥”∞±¥şªØ—ªØø…“‘÷∆œÀ·£¨¥Àπ˝≥Ã÷–…ʺ∞µ™—ªØŒÔ£¨»ÁNO°¢NO2°¢N2O4µ»°£∂‘∑¥”¶? N2O4£®g£©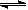 2NO2£®g£©? °˜H>0£¨‘ĞŒ¬∂»Œ™T1°¢T2 ±£¨∆Ω∫‚ÃÂœµ÷–NO2µƒÃª˝∑÷ ˝ÀÊ—π«ø±‰ªØ«˙œş»ÁÕºÀ˘ æ°£œ¬¡–Àµ∑®’˝»∑µƒ «___________°£
2NO2£®g£©? °˜H>0£¨‘ĞŒ¬∂»Œ™T1°¢T2 ±£¨∆Ω∫‚ÃÂœµ÷–NO2µƒÃª˝∑÷ ˝ÀÊ—π«ø±‰ªØ«˙œş»ÁÕºÀ˘ æ°£œ¬¡–Àµ∑®’˝»∑µƒ «___________°£

A£ÆA°¢C¡Ωµ„µƒ∑¥”¶ÀŸ¬ £∫A£æC
B£ÆA°¢C¡Ωµ„∆¯Ãµƒ—’…´£∫A…Ó£¨C«≥
C£ÆB°¢C¡Ωµ„µƒ∆¯Ãµƒ∆Ωæ˘œ‡∂‘∑÷◊”÷ ¡ø£∫B£ºC
D£Æ”…◊¥Ã¨BµΩ◊¥Ã¨A£¨ø…“‘”√º”»»µƒ∑Ω∑®
E£ÆA°¢C¡Ωµ„µƒªØ—ß∆Ω∫‚≥£ ˝£∫A£æC
£®5£©NO2ø…”√∞±ÀÆŒ¸ ’…˙≥…NH4NO3 °£25°Ê ±£¨Ω´m mol NH4NO3»İ”ĞÀÆ£¨»İ“∫œ‘À·–‘£¨œÚ∏√»İ“∫µŒº”n L∞±ÀÆ∫ۻݓ∫≥ ÷––‘£¨‘ÚµŒº”∞±ÀƵƒπ˝≥Ã÷–ÀƵƒµÁ¿Î∆Ω∫‚Ω´______£®ÃÓ°±’˝œÚ°±°∞≤ª°±ªÚ°∞ƒÊœÚ°±£©“∆∂Ø£¨À˘µŒº”∞±ÀƵƒ≈®∂»Œ™_______mol°§L-1°££®NH3°§H2OµƒµÁ¿Î∆Ω∫‚≥£ ˝»°Kb=2X10-5 mol°§L-1£©
£®6£©ƒ≥ø∆—–µ•Œª¿˚”√‘≠µÁ≥ÿ‘≠¿Ì£¨”√SO2∫ÕO2¿¥÷∆±∏¡ÚÀ·£¨◊∞÷√»Á”“Õº£¨µÁº´Œ™∂‡ø◊µƒ≤ƒ¡œƒİŒ¸∏Ω∆¯Ã£¨Õ¨ ±“≤ƒİ π∆¯Ã”εÁΩ‚÷ »İ“∫≥‰∑÷Ω”¥•£Æ

¢Ÿ»İ“∫÷–H+µƒ“∆∂Ø∑ΩœÚ”…______ º´µΩ______º´£ª£®”√A°¢B±Ì 棩
¢ĞBµÁº´µƒµÁº´∑¥”¶ ΩŒ™__________________________°£
£®6∑÷£©œ¬¡–Àµ∑®’˝»∑µƒ « £®ÃÓ–Ú∫≈£©°£
¢Ÿ”…”е‚‘Ğæ∆æ´÷–µƒ»İΩ‚∂»¥Û£¨À˘“‘ø…”√æ∆æ´Ω´µ‚ÀÆ÷–µƒµ‚ıÕ»°≥ˆ¿¥
¢ĞÀƵƒ∑–µ„ «100°Ê£¨æ∆æ´µƒ∑–µ„ «78.5°Ê£¨”√÷±Ω”’Ù¡Û∑®ƒİ π∫¨ÀÆæ∆æ´±‰Œ™ŒŞÀÆæ∆æ´
¢ğ”…”ĞΩ∫¡£µƒ÷±æ∂±»¿Î◊”¥Û£¨À˘“‘µÌ∑ğ»İ“∫÷–ªÏ”–µƒµ‚ªØºÿø…”√…¯Œˆ∑®∑÷¿Î
¢İ∑÷¿Î±Ω∫Õ±Ω∑”µƒªÏ∫œ“∫£¨œ»º”»Î ¡ø≈®‰ÂÀÆ£¨‘Ÿπ˝¬À°¢∑÷“∫£¨º¥ø… µœ÷
¢ı”…”Ğ∏şº∂÷¨∑æÀ·ƒ∆—Œ‘ĞÀÆ÷–µƒ∑÷…¢÷ Œ¢¡£÷±æ∂‘Ğ1nm°´100 nm÷ƺ‰£¨À˘“‘ø…”√ ≥—Œ π∏şº∂÷¨∑æÀ·ƒ…¥”‘̪Ø∑¥”¶∫ÛµƒªÏ∫œŒÔ÷–Œˆ≥ˆ
¢Ş≤ª…˜∞—±Ω∑”»İ“∫’¥µΩ∆§∑Ù…œ£¨”¶¡¢º¥”√æ∆æ´œ¥µ”
¢ş”√œ°‰ÂÀƵŒ»Î±Ω∑”»İ“∫÷–÷∆±∏2£¨4£¨6£≠»˝‰Â±Ω∑”
¢‡ µ—È “ π”√ê˝±»Œ™1:3µƒ≈®¡ÚÀ·”Γ“¥ºµƒªÏ∫œ»İ“∫÷∆““œ© ±£¨Œ™∑¿º”»» ±∑¥”¶ªÏ∫œ“∫≥ˆœ÷±©∑–œ÷œÛ£¨≥˝¡À“™º”∑– ØÕ‚£¨ªπ”¶◊¢“‚ª∫¬˝º”»»»√Œ¬∂»¬˝¬˝…˝÷¡170°Ê
17£Æ.(18∑÷)ƒ≥ªØ—ß–°◊È≤…”√¿‡À∆÷∆““À·““•µƒ◊∞÷√£®»Á”“Õº£©£¨“‘ª∑º∫¥º÷∆±∏ª∑º∫œ©£∫
 “—÷™£∫
“—÷™£∫
| √İ∂» | »ğµ„ | ∑–µ„ | »İΩ‚–‘ | |
| ª∑º∫¥º | 0.96 | 25 | 161 | ƒİ»İ”ĞÀÆ |
| ª∑º∫œ© | 0.81 | £≠103 | 83 | ƒ—»İ”ĞÀÆ |
£®1£©÷∆±∏¥÷∆∑
Ω´12.5mLª∑º∫¥ºº”»Î ‘πİA÷–£¨‘Ÿº”»Î1mL≈®¡ÚÀ·£¨“°‘»∫Û∑≈»ÎÀÈ¥…∆¨£¨ª∫¬˝º”»»÷¡∑¥”¶ÕÍ»´£¨‘Ğ ‘πİCƒĞµ√µΩª∑º∫œ©¥÷∆∑°£
¢ŸA÷–ÀÈ¥…∆¨µƒ◊˜”√ « £¨
µºπİB≥˝¡Àµº∆¯Õ‚ªπæş”–µƒ◊˜”√ « °£
¢Ğ ‘πİC÷√”б˘ÀÆ‘°÷–µƒƒøµƒ « °£
 £®2£©÷∆±∏æ´∆∑
£®2£©÷∆±∏æ´∆∑
¢Ÿª∑º∫œ©¥÷∆∑÷–∫¨”–ª∑º∫¥º∫Õ…Ÿ¡øÀ·–‘‘”÷ µ»°£º”»Î±•∫Õ
≥—ŒÀÆ£¨’Òµ¥°¢æ≤÷√°¢∑÷≤„£¨ª∑º∫œ©‘Ğ ≤„£®ÃÓ
°∞…œ°±ªÚ°∞œ¬°±£©£¨∑÷“∫∫Û”√ £®Ãӻα‡∫≈£©œ¥µ”°£
A£ÆKMnO4»İ“∫ B£Æœ°H2SO4 C£ÆNa2CO3»İ“∫
¢Ğ‘ŸΩ´ª∑º∫œ©∞¥”“Õº◊∞÷√’Ù¡Û£¨¿‰»¥ÀÆ¥” øĞΩ¯»Î°£
’Ù¡Û ±“™º”»Î…˙ ت“£¨ƒøµƒ «:°°°° °°°° °£
¢ğ ’ºØ≤˙∆∑ ±£¨øÿ÷∆µƒŒ¬∂»”¶‘Ğ ◊Û”“£¨ µ—È÷∆µ√µƒª∑º∫œ©æ´∆∑÷ ¡øµÕ”п̬ğ≤˙¡ø£¨ø…ƒİµƒ‘≠“Ú « £® £©
A£Æ’Ù¡Û ±¥”70°Êø™ º ’ºØ≤˙∆∑ B£Æª∑º∫¥º µº ”√¡ø∂‡¡À
C£Æ÷∆±∏¥÷∆∑ ±ª∑º∫¥ºÀÊ≤˙∆∑“ª∆’Ù≥ˆ
£®3£©“‘œ¬«¯∑÷ª∑º∫œ©æ´∆∑∫Õ¥÷∆∑µƒ∑Ω∑®£¨∫œ¿Ìµƒ « ( )
A£Æ”√À·–‘∏ş√ÃÀ·ºÿ»İ“∫ B£Æ”√Ω Ùƒ∆ C£Æ≤‚∂®∑–µ„
18£Æ£®12∑÷£©”–ª˙
ŒÔAµƒΩ·ππºÚ ΩŒ™![]() £¨À¸ø…Õ®π˝≤ªÕ¨ªØ—ß∑¥”¶∑÷±÷∆µ√B°¢C°¢D∫ÕEÀƒ÷÷ŒÔ÷ °£
£¨À¸ø…Õ®π˝≤ªÕ¨ªØ—ß∑¥”¶∑÷±÷∆µ√B°¢C°¢D∫ÕEÀƒ÷÷ŒÔ÷ °£

«Îªÿ¥œ¬¡–Œ £∫
£®1£©÷∏≥ˆ∑¥”¶µƒ¿‡–Õ£∫A°˙C£∫ °£
£®2£©‘ĞA~EŒÂ÷÷ŒÔ÷ ÷–£¨ª•Œ™Õ¨∑÷“Ïππõƒ « £®ÃÓ¥˙∫≈£©°£
£®3£©–¥≥ˆ”…A…˙≥…BµƒªØ—ß∑Ω≥à Ω
°£
£®4£©“—÷™HCHO∑÷◊”÷–À˘”–‘≠◊”∂º‘ĞÕ¨“ª∆Ω√ʃУ¨‘Ú‘Ğ…œ ˆ∑÷◊”÷–À˘”–µƒ‘≠◊””–ø…ƒİ∂º‘ĞÕ¨“ª∆Ω√ʵƒŒÔ÷ « £®ÃÓ–Ú∫≈£©°£
£®5£©Cƒİ–Œ≥…∏şæğŒÔ£¨∏√∏şæğŒÔµƒΩ·ππºÚ ΩŒ™ °£
£®6£©–¥≥ˆD”ÎNaOH»İ“∫π≤»»∑¥”¶µƒªØ—ß∑Ω≥à Ω
°£
19.£®16∑÷£©»‚
πÀ·º◊•£® £©≥£”√”е˜÷∆æş”–≤ııÆ°¢∆œÃ—°¢”£Ã“°¢œ„◊”¿ºµ»œ„Œ∂µƒ ≥”√œ„æ´
£©≥£”√”е˜÷∆æş”–≤ııÆ°¢∆œÃ—°¢”£Ã“°¢œ„◊”¿ºµ»œ„Œ∂µƒ ≥”√œ„æ´
¢≈»‚πÀ·º◊•µƒ∑÷◊” Ω « £ª
 ¢∆œ¬¡–”–πÿ»‚πÀ·º◊•µƒ– ˆ÷–£¨’˝»∑µƒ « ÃÓ◊÷ƒ∏£©£ª
¢∆œ¬¡–”–πÿ»‚πÀ·º◊•µƒ– ˆ÷–£¨’˝»∑µƒ « ÃÓ◊÷ƒ∏£©£ª
A£Æƒİ”ΉµƒÀƒ¬»ªØú»İ“∫∑¢…˙º”≥…∑¥”¶
B£ÆŒŞ∑® πÀ·–‘∏ş√ÃÀ·ºÿ»İ“∫Õ …´
C£Æ‘кӖ‘ú˛œ¬ƒİ∑¢…˙ÀÆΩ‚∑¥”¶
D£Æ≤ªø…ƒİ∑¢…˙º”æğ∑¥”¶
¢«GŒ™»‚πÀ·º◊•µƒ“ª÷÷Õ¨∑÷“Ïππã¨∆‰∑÷◊”Ω·ππƒ£–Õ»Á”“ÕºÀ˘ 森պ÷–«Ú”ΫÚ÷ƺ‰¡¨œş±Ì 浕º¸ªÚÀ´º¸£©°£‘ÚGµƒΩ·ππºÚ ΩŒ™ £ª
¢»”√∑ºœ„Ã˛AŒ™‘≠¡œ∫œ≥…Gµƒ¬∑œş»Áœ¬£∫

¢ŸªØ∫œŒÔE÷–µƒπŸƒİÕ≈”– £®ÃÓ√˚≥∆£©°£
¢ĞF°˙Gµƒ∑¥”¶¿‡–Õ « £¨∏√∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™ _ _ °£
¢ğC°˙DµƒªØ—ß∑Ω≥Ã ΩŒ™ _°£
¢İ–¥≥ˆ∑˚∫œœ¬¡–ú˛µƒFµƒÕ¨∑÷“ÏππõƒΩ·ππºÚ Ω °£O%M
¢°£Æ∑÷◊”ƒĞ∫¨±Ωª∑£¨«“±Ωª∑…œ÷ª”–“ª∏ˆ÷ß¡¥£ª
¢¢£Æ“ª∂®Ãº˛œ¬£¨1mol∏√ŒÔ÷ ”Î◊„¡ø“¯∞±»İ“∫≥‰∑÷∑¥”¶£¨…˙≥…4mol“¯µ•÷ °£
20£Æ£®10∑÷£©”–ª˙ŒÔAµƒ’Ù∆˚∂‘Õ¨Œ¬Õ¨—πœ¬«‚∆¯µƒœ‡∂‘√İ∂»Œ™31£¨»°3.1øÀAŒÔ÷ ‘Ğ◊„¡ø—∆¯÷–≥‰∑÷»º…’£¨÷ª…˙≥…2.7øÀÀÆ∫Õ±Í◊º◊¥øˆœ¬CO22.24L£¨«Û”–ª˙ŒÔµƒ∑÷◊” Ω£ª»Ù∏√”–ª˙ŒÔ0.2mol«°∫√”Î9.2øÀΩ Ùƒ∆ÕÍ»´∑¥”¶£¨«Î–¥≥ˆ”–ª˙ŒÔµƒΩ·ππºÚ Ω≤¢√¸√˚°£
“—÷™¥◊À·∫Õ—ŒÀ· «»’≥£…˙ªÓ÷–º´Œ™≥£º˚µƒÀ·£¨‘Ğ“ª∂®Ãº˛œ¬£¨CH3COOH»İ“∫÷–¥Ê‘еÁ¿Î∆Ω∫‚£∫CH3COOH ![]() CH3COO£≠+H+ £ª¶§H>0
CH3COO£≠+H+ £ª¶§H>0
£®1£©25 °Ê ±£¨≈®∂»æ˘Œ™0.1mol/Lµƒ—ŒÀ·∫Õ¥◊À·»İ“∫£¨œ¬¡–Àµ∑®’˝»∑µƒ « £ª
¢Ÿ¡Ω»İ“∫µƒpHœ‡Õ¨
¢Ğ¡Ω»İ“∫µƒµºµÁƒİ¡¶œ‡Õ¨
¢ğ”…ÀƵÁ¿Î≥ˆµƒc(OH£≠)œ‡Õ¨
 ¢İ÷–∫Õµ»ŒÔ÷ µƒ¡øµƒNaOH»İ“∫£¨œ˚∫ƒ¡Ω»İ“∫µƒÃª˝œ‡Õ¨
¢İ÷–∫Õµ»ŒÔ÷ µƒ¡øµƒNaOH»İ“∫£¨œ˚∫ƒ¡Ω»İ“∫µƒÃª˝œ‡Õ¨
£®2£©25 °Ê ±£¨œÚpHæ˘Œ™1µƒ—ŒÀ·∫Õ¥◊À·»İ“∫÷–∑÷±º”ÀÆ£¨Àʺ”ÀÆ
¡øµƒ‘ˆ∂‡£¨¡Ω»İ“∫pHµƒ±‰ªØ»ÁÕºÀ˘ 棨‘Ú∑˚∫œ—ŒÀ·pH±‰ªØ
µƒ«˙œş « £ª
£®3£©25 °Ê ±£¨œÚê˝Œ™Va mL pH=3µƒ¥◊À·»İ“∫÷–µŒº”pH=11µƒ
NaOH»İ“∫Vb mL÷¡»İ“∫«°∫√≥ ÷––‘£¨‘ÚVa Vb£®ÃÓ°∞£æ°±°¢°∞£º°±ªÚ°∞£Ω°±£©
ºŸ…Ë÷ ºÏ≤ø√≈πÊ∂® – ğ¥◊À·≈®∂»≤ªµ√µÕ”Ğ4.8g/100mL£¨ƒ≥Õ¨—ß”˚”√÷–∫ÕµŒ∂®µƒ∑Ω∑®¿¥≤‚∂®ƒ≥∆∑≈∆µƒ ≥”√¥◊÷–µƒ¥◊À·∫¨¡ø «∑ҥԱͰ£ µ—ÈæşÃÂ≤Ω÷Ë»Áœ¬£∫¢ŸÕ–≈ÃÃÏ∆Ω≥∆»°“ª∂®÷ ¡øNaOH≤¢≈‰÷∆≥…500mL NaOH»İ“∫£ª¢Ğ”√“—÷™≈®∂»µƒ—ŒÀ·±Í◊º»İ“∫◊º»∑±Í∂®∏√NaOH»İ“∫µƒ≈®∂»£ª¢ğ”√…œ ˆ“—÷™◊º»∑≈®∂»µƒNaOH»İ“∫≤‚∂®¥◊À·µƒ≈®∂»°£
£®4£©≤ª÷±Ω””√≈‰÷√µƒNaOH»İ“∫µŒ∂®—˘∆∑£¨∂¯“™”√±Í◊º—ŒÀ·œ»±Í∂®‘ŸµŒ∂®µƒ‘≠“Ú « £ª
£®5£©»Ù µ—Èπ˝≥ûÁœ¬£∫◊º»∑¡ø»°∏√ ≥”√¥◊20.00mL£¨÷√”Ğ250mL◊∂–Œ∆ø÷–£¨‘ŸµŒº”∑”Ù÷∏ 溡£¨”√±Í∂®∫√µƒ0.1000mol/LµƒNaOH»İ“∫µŒ∂®£¨∑”Ù÷∏ 溡”… …´«°∫√±‰≥…__________…´«“ º¥Œ™÷’µ„°£
÷ÿ∏¥µŒ∂®∂‡¥Œ£¨Ω·π˚º«¬º»Áœ¬£∫
| ≤‚∂®¥Œ–Ú | µĞ“ª¥Œ | µĞ∂˛¥Œ | µĞ»˝¥Œ | µĞÀƒ¥Œ |
| V£®mL£© | 19.40 | 15.10 | 14.90 | 15.00 |
‘Ú∏√ ≥”√¥◊÷–¥◊À·µƒŒÔ÷ µƒ¡ø≈®∂»£Ω________ mol°§L£≠1£¨ «∑Ò∫œ∏Ò £®ÃÓ°± «°±ªÚ°±∑Ò°±£©
µ•æßπË «–≈œ¢≤˙“µ÷–÷ÿ“™µƒª˘¥°≤ƒ¡œ£ÆÕ®≥£”√Ãø‘Ğ∏şŒ¬œ¬ªπ‘≠∂˛—ªØπË÷∆µ√¥÷πË(∫¨Ã˙°¢¬¡°¢≈°¢¡◊µ»‘”÷ )£¨¥÷π˔ά»∆¯∑¥”¶…˙≥…Àƒ¬»ªØπË(∑¥”¶Œ¬∂»450~500°Ê)£¨Àƒ¬»ªØπËæ≠÷¥ø∫Û”√«‚∆¯ªπ‘≠ø…µ√∏ş¥øπˣƓ‘œ¬ « µ—È ““‘¥÷πË÷∆±∏Àƒ¬»ªØπ˵ƒ◊∞÷√ æ“‚Õº
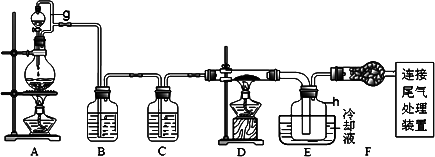
œ‡πÿ–≈œ¢»Áœ¬£∫¢ŸÀƒ¬»ªØπË”ˆÀƺ´“◊ÀÆΩ‚£ª
¢Ğ≈°¢¬¡°¢Ã˙°¢¡◊‘Ğ∏şŒ¬œ¬æ˘ƒİ”ά»∆¯÷±Ω”∑¥”¶…˙≥…œ‡”¶µƒ¬»ªØŒÔ£ª
¢ğ”–πÿŒÔ÷ µƒŒÔ¿Ì≥£ ˝º˚œ¬±Ì£∫
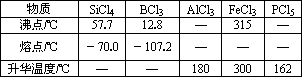
«Îªÿ¥œ¬¡–Œ £∫
(1)◊∞÷√A÷–◊∞µƒ∑¥”¶ŒÔŒ™≈®—ŒÀ·”Î∂˛—ªØ√㨖¥A÷–∑¢…˙∑¥”¶µƒ¿Î◊”∑Ω≥à Ω________£Æ
(2)◊∞÷√A÷–gπݵƒ◊˜”√ «________£ª◊∞÷√C÷–µƒ ‘º¡ «________£Æ
(3)◊∞÷√E÷–h∆ø ’ºØµΩµƒ¥÷≤˙ŒÔø…Õ®π˝æ´¡Û(¿‡À∆∂‡¥Œ’Ù¡Û)µ√µΩ∏ş¥ø∂»Àƒ¬»ªØπË£¨æ´¡Û∫Ûµƒ≤–¡ÙŒÔ÷–£¨≥˝Ã˙‘™ÀÿÕ‚ø…ƒİªπ∫¨”–µƒ‘”÷ ‘™Àÿ «________(ÃÓ–¥‘™Àÿ∑˚∫≈)£Æ
(4)Œ™¡À∑÷Œˆ≤–¡ÙŒÔ÷–Ã˙‘™Àÿµƒ∫¨¡ø£¨œ»Ω´≤–¡ÙŒÔ‘§¥¶¿Ì£¨ πÃ˙‘™Àÿªπ‘≠≥…Fe2
+£¨‘Ÿ”√KMnO4±Í◊º»İ“∫‘ĞÀ·–‘ú˛œ¬Ω¯––—ªØªπ‘≠µŒ∂®£¨∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω «£∫5Fe2+£´MnO4£≠£´8H+¢ŸµŒ∂®«∞ «∑Ò“™µŒº”÷∏ 溡£ø________(ÃÓ°∞ «°±ªÚ°∞∑Ò°±)£¨«ÎÀµ√˜¿Ì”…________£Æ
¢Ğƒ≥Õ¨—ß≥∆»°5.000 g≤–¡ÙŒÔ∫Û£¨æ≠‘§¥¶¿Ì∫Û‘Ğ»ı¡ø∆ø÷–≈‰÷∆≥…100 mL»İ“∫£¨“∆»°25.00 mL ‘—˘»İ“∫£¨”√1.000°¡10£≠2 mol/L°°KMnO4±Í◊º»İ“∫µŒ∂®£Æ¥ÔµΩµŒ∂®÷’µ„ ±£¨œ˚∫ƒ±Í◊º»İ“∫20.00 mL£¨‘Ú≤–¡ÙŒÔ÷–Ã˙‘™Àÿµƒ÷ ¡ø∑÷ ˝ «________
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒŞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com