
题目列表(包括答案和解析)
已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO3- + H2O H2SO3 + OH- ①
HSO3- H+ + SO32- ②
向0.1mol·L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是
A. 加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大
B. 加入少量Na2SO3固体,则c(H+) + c(Na+) = c(HSO3-) + c(OH-) +![]() c(SO32-)
c(SO32-)
C. 加入少量NaOH溶液,![]() 、
、![]() 的值均增大
的值均增大
D. 加入氨水至中性,则2c(Na+) = c(SO32-)>c(H+) = c(OH-)
已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO3-+ H2O  H2SO3 + OH- ①
H2SO3 + OH- ①
HSO3- H+ + SO32- ②
H+ + SO32- ②
向0.1mol·L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是
A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大
B.加入少量Na2SO3固体,则c(H+) + c(Na+) = c(HSO3-)
+ c(OH-) + c(SO32-)
c(SO32-)
C.加入少量NaOH溶液, 、
、 的值均增大
的值均增大
D.加入氨水至中性,则2c(Na+) = c(SO32-)>c(H+) = c(OH-)
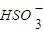 +H2O?H2SO3+OH-①
+H2O?H2SO3+OH-①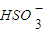 ?H++
?H++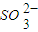 ②,向0.1mol?L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是( )
②,向0.1mol?L-1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是( )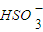 )增大
)增大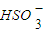 )+c(OH-)+
)+c(OH-)+ c(
c(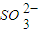 )
)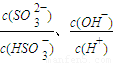 的值均增大
的值均增大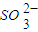 )>c(H+)=c(OH-)
)>c(H+)=c(OH-) H2SO3 + OH- ①
H2SO3 + OH- ① H+ + SO32- ②
H+ + SO32- ②| A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大 |
B.加入少量Na2SO3固体,则c(H+) + c(Na+) = c(HSO3-) + c(OH-) +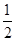 c(SO32-) c(SO32-) |
C.加入少量NaOH溶液,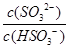 、 、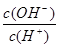 的值均增大 的值均增大 |
| D.加入氨水至中性,则2c(Na+) = c(SO32-)>c(H+) = c(OH-) |
| A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3-)增大 |
| B.加入少量Na2SO3固体,则c(H+)+c(Na+)=c(HSO3-)+c(OH-)+2c(SO32-) |
| C.加入一定量的蒸馏水,溶液中c(H+)和c(OH-)都减少 |
| D.加入氨水至中性,则2c(Na+)=c(SO32-)>c(H+)=c(OH-) |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com