
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
ÄæĒ°¹¤ŅµŗĻ³É°±µÄŌĄķŹĒ£ŗN2(g)+3H2(g) 2NH3(g)
”÷H=£93.0kJ /mol£»Įķ¾Ż±ØµĄ£¬Ņ»¶ØĢõ¼žĻĀ£ŗ2N2(g)+6H2O(l)
2NH3(g)
”÷H=£93.0kJ /mol£»Įķ¾Ż±ØµĄ£¬Ņ»¶ØĢõ¼žĻĀ£ŗ2N2(g)+6H2O(l) 4NH3(g)+3O2(g)
”÷H= +1530.0kJ /mol”£
4NH3(g)+3O2(g)
”÷H= +1530.0kJ /mol”£
£Ø1£©ĒāĘųµÄČ¼ÉÕČČ”÷H=_______________kJ/mol”£
£Ø2£©ŌŚŗćĪĀŗćŃ¹×°ÖĆÖŠ½ųŠŠ¹¤ŅµŗĻ³É°±·“Ó¦£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ ”£
A£®ĘųĢåĢå»ż²»ŌŁ±ä»Æ£¬ŌņŅŃĘ½ŗā
B£®ĘųĢåĆÜ¶Č²»ŌŁ±ä»Æ£¬ÉŠĪ“Ę½ŗā
C£®Ę½ŗāŗó£¬Ķł×°ÖĆÖŠĶØČėŅ»¶ØĮæAr£¬Ń¹Ēæ²»±ä£¬Ę½ŗā²»ŅʶÆ
D£®Ę½ŗāŗó£¬Ń¹Ėõ×°ÖĆ£¬Éś³Éøü¶ąNH3
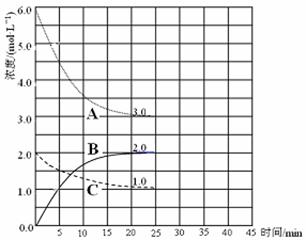
£Ø3£©ŌŚŗćĪĀŗćȯװÖĆÖŠ½ųŠŠŗĻ³É°±·“Ó¦£¬ø÷×é·ÖÅضČ-Ź±¼äĶ¼ĻńČēĻĀ”£
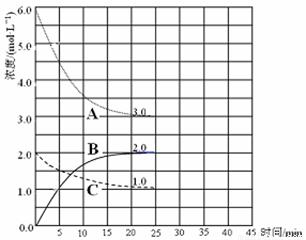
¢Ł ±ķŹ¾N2ÅØ¶Č±ä»ÆµÄĒśĻߏĒ ”£
¢Ś Ē°25 min ÄŚ£¬ÓĆH2ÅØ¶Č±ä»Æ±ķŹ¾µÄ»Æѧ·“Ó¦ĖŁĀŹŹĒ ”£
¢Ū ŌŚ25 minÄ©øÕŗĆĘ½ŗā£¬ŌņĘ½ŗā³£ŹżK = ”£
£Ø4£©ŌŚµŚ25 min Ä©£¬±£³ÖĘäĖüĢõ¼ž²»±ä£¬ÉżøßĪĀ¶Č£¬ŌŚµŚ35 minÄ©ŌŁ“ĪĘ½ŗā”£Ę½ŗāŅĘ¶Æ¹ż³ĢÖŠH2ÅØ¶Č±ä»ÆĮĖ1.5 mol”¤L£1£¬ŌŚĶ¼ÖŠ»³öµŚ25 min ”« 40 min NH3ÅØ¶Č±ä»ÆĒśĻß”£
£Ø5£©ŅŃÖŖ³£ĪĀĻĀ£¬NH4+ µÄĖ®½ā³£ŹżĪŖ1.0”Į10£9£¬Ōņ0.1mol/L NH4ClČÜŅŗpH= ”££ØŗöĀŌNH4+Ė®½ā¶ŌNH4+ÅØ¶ČµÄÓ°Ļģ£©
ÄæĒ°¹¤ŅµŗĻ³É°±µÄŌĄķŹĒ£ŗN2(g)+3H2(g) 2NH3(g) ”÷H=£93.0kJ /mol£»Įķ¾Ż±ØµĄ£¬Ņ»¶ØĢõ¼žĻĀ£ŗ2N2(g)+6H2O(l)
2NH3(g) ”÷H=£93.0kJ /mol£»Įķ¾Ż±ØµĄ£¬Ņ»¶ØĢõ¼žĻĀ£ŗ2N2(g)+6H2O(l) 4NH3(g)+3O2(g) ”÷H=" +1530.0kJ" /mol”£
4NH3(g)+3O2(g) ”÷H=" +1530.0kJ" /mol”£
£Ø1£©ĒāĘųµÄČ¼ÉÕČČ”÷H=_______________kJ/mol”£
£Ø2£©ŌŚŗćĪĀŗćŃ¹×°ÖĆÖŠ½ųŠŠ¹¤ŅµŗĻ³É°±·“Ó¦£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ ”£
| A£®ĘųĢåĢå»ż²»ŌŁ±ä»Æ£¬ŌņŅŃĘ½ŗā |
| B£®ĘųĢåĆÜ¶Č²»ŌŁ±ä»Æ£¬ÉŠĪ“Ę½ŗā |
| C£®Ę½ŗāŗó£¬Ķł×°ÖĆÖŠĶØČėŅ»¶ØĮæAr£¬Ń¹Ēæ²»±ä£¬Ę½ŗā²»ŅĘ¶Æ |
| D£®Ę½ŗāŗó£¬Ń¹Ėõ×°ÖĆ£¬Éś³Éøü¶ąNH3 |
 2NH3(g) ”÷H=£93.0kJ /mol£»Įķ¾Ż±ØµĄ£¬Ņ»¶ØĢõ¼žĻĀ£ŗ2N2(g)+6H2O(l)
2NH3(g) ”÷H=£93.0kJ /mol£»Įķ¾Ż±ØµĄ£¬Ņ»¶ØĢõ¼žĻĀ£ŗ2N2(g)+6H2O(l) 4NH3(g)+3O2(g) ”÷H=" +1530.0kJ" /mol”£
4NH3(g)+3O2(g) ”÷H=" +1530.0kJ" /mol”£| A£®ĘųĢåĢå»ż²»ŌŁ±ä»Æ£¬ŌņŅŃĘ½ŗā |
| B£®ĘųĢåĆÜ¶Č²»ŌŁ±ä»Æ£¬ÉŠĪ“Ę½ŗā |
| C£®Ę½ŗāŗó£¬Ķł×°ÖĆÖŠĶØČėŅ»¶ØĮæAr£¬Ń¹Ēæ²»±ä£¬Ę½ŗā²»ŅĘ¶Æ |
| D£®Ę½ŗāŗó£¬Ń¹Ėõ×°ÖĆ£¬Éś³Éøü¶ąNH3 |
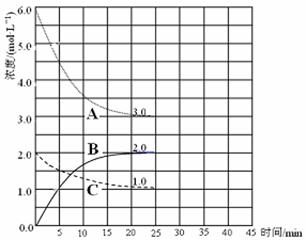
£Ø7·Ö£©Ņ»¶ØĢõ¼žĻĀ£¬ŌŚĢå»żĪŖ3LµÄĆܱÕČŻĘ÷ÖŠ£¬Ņ»Ńõ»ÆĢ¼ÓėĒāĘų·“Ӧɜ³É¼×“¼£Ø“߻ƼĮĪŖCu2O/ZnO£©£ŗCO£Øg£©£«2H2£Øg£©CH3OH£Øg£© ¦¤H< 0
øł¾ŻĢāŅāĶź³ÉĻĀĮŠø÷Ģā£ŗ
£Ø1£©·“Ó¦“ļµ½Ę½ŗāŹ±£¬Ę½ŗā³£Źż±ķ“ļŹ½K £½ ”£
£Ø2£©ĘäĖüĢõ¼ž²»±ä£¬½ö°ŃĪĀ¶ČøÄĪŖ500”ę£¬ĒėŌŚĻĀĶ¼ÉĻ»³ö“ĖĪĀ¶ČĻĀ¼×“¼µÄĪļÖŹµÄĮæĖę·“Ó¦Ź±¼ä±ä»ÆµÄŹ¾ŅāĶ¼”£
£Ø3£©ÉżøßĪĀ¶Č£¬KÖµ £ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©£¬Ōö“óŃ¹Ē棬
KÖµ £ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©”£
£Ø4£©ŌŚ300”ę£¬“Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ĒāĘųµÄĘ½¾ł·“Ó¦ĖŁĀŹv£ØH2£©£½
£Ø5£©ŌŚĘäĖūĢõ¼ž²»±äµÄĒéæöĻĀ£¬¶Ō“¦ÓŚBµćµÄĢåĻµĢå»żŃ¹Ėõµ½ŌĄ“µÄ1/2£¬ĻĀĮŠÓŠ¹ŲøĆĢåĻµµÄĖµ·ØÕżČ·µÄŹĒ£Ø £©
a£®ĒāĘųµÄÅØ¶Č¼õÉŁ b£®Õż·“Ó¦ĖŁĀŹ¼Óæģ£¬Äę·“Ó¦ĖŁĀŹ¼õŠ”
c£®¼×“¼µÄĪļÖŹµÄĮæŌö¼Ó d£®ÖŲŠĀĘ½ŗāŹ±n£ØH2£©/n£ØCH3OH£©¼õŠ”
£Ø7·Ö£©Ņ»¶ØĢõ¼žĻĀ£¬ŌŚĢå»żĪŖ3LµÄĆܱÕČŻĘ÷ÖŠ£¬Ņ»Ńõ»ÆĢ¼ÓėĒāĘų·“Ӧɜ³É¼×“¼£Ø“߻ƼĮĪŖCu2O/ZnO£©£ŗCO£Øg£©£«2H2£Øg£© CH3OH£Øg£© ¦¤H< 0
CH3OH£Øg£© ¦¤H< 0
øł¾ŻĢāŅāĶź³ÉĻĀĮŠø÷Ģā£ŗ
£Ø1£©·“Ó¦“ļµ½Ę½ŗāŹ±£¬Ę½ŗā³£Źż±ķ“ļŹ½K £½ ”£
£Ø2£©ĘäĖüĢõ¼ž²»±ä£¬½ö°ŃĪĀ¶ČøÄĪŖ500”ę£¬ĒėŌŚĻĀĶ¼ÉĻ»³ö“ĖĪĀ¶ČĻĀ¼×“¼µÄĪļÖŹµÄĮæĖę·“Ó¦Ź±¼ä±ä»ÆµÄŹ¾ŅāĶ¼”£
£Ø3£©ÉżøßĪĀ¶Č£¬KÖµ £ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©£¬Ōö“óŃ¹Ē棬
KÖµ £ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©”£
£Ø4£©ŌŚ300”ę£¬“Ó·“Ó¦æŖŹ¼µ½Ę½ŗā£¬ĒāĘųµÄĘ½¾ł·“Ó¦ĖŁĀŹv£ØH2£©£½
£Ø5£©ŌŚĘäĖūĢõ¼ž²»±äµÄĒéæöĻĀ£¬¶Ō“¦ÓŚBµćµÄĢåĻµĢå»żŃ¹Ėõµ½ŌĄ“µÄ1/2£¬ĻĀĮŠÓŠ¹ŲøĆĢåĻµµÄĖµ·ØÕżČ·µÄŹĒ£Ø £©
a£®ĒāĘųµÄÅØ¶Č¼õÉŁ b£®Õż·“Ó¦ĖŁĀŹ¼Óæģ£¬Äę·“Ó¦ĖŁĀŹ¼õŠ”
c£®¼×“¼µÄĪļÖŹµÄĮæŌö¼Ó d£®ÖŲŠĀĘ½ŗāŹ±n£ØH2£©/n£ØCH3OH£©¼õŠ”
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com