
题目列表(包括答案和解析)
原子是由 、 构成的。原子的质量主要集中在 上。
(12分)构成物质的微粒很多,离子就是构成物质的基本微粒之一,下表是中学化学中常见的几种离子:
回答下列问题:
(1)K+离子的结构示意图 ,Cl在周期表中的位置是 。
(2)将含OH-离子的溶液滴入浓度为0.1mol/L的Al3+和NH+4的混合溶液中,若测得溶液中NH+4减少了一半,则此时溶液中 (填“存在”或“不存在”)大量的Al3+。
(3)物质A和B分别由上表中的两种离子组成,将它们分别溶于水中,A的溶液显酸性,B的溶液显碱性且B的焰色反应呈紫色(透过蓝色钻玻璃观察),将A、B两溶液混合,既有白色沉淀生成,又有无色无味的气体生成。则A中含有的阳离子是 ,B溶液显碱性的原因是(用离子方程式和必要的文字说明) 。
(4)常温下,将(NH4)2CO3溶于水,得到含有大量NH4+和CO2-3的溶液,往溶液中滴入少量氨水,测得溶液中NH+4和CO2-3的浓度比为2:1,则此时该溶液的pH (填“<”、 “=”或“>”)7。
(5)在微生物作用下的条件,NH+4可被空气氧化成NO-3。写出该反应的离子方程式
。
(12分)原子序数由小到大排列的X、Y、Z三种短周期元素,已知三种元素的原子序数之和等于16, 单质X2 、Y2 、Z2之间有如下转化关系(反应条件已略)。已知:甲、乙分子中均含有10个电子;丙分子中含有15个电子。请回答:
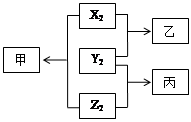
(1)Y2的电子式是___ ______;该分子中有 个σ键, 个π键。
(2)甲属于(填“极性”或“非极性”) 分子;晶体中甲分子的配位数为 。
(3)乙分子的VSEPR模型名称为 ,分子的立体构型名称为 。
(4)写出乙与Z2反应生成丙的化学方程式 。
(5)工业上用氧化铝、碳和乙在1400℃条件下反应,制取由元素Y和Al组成的化合物丁,同时还有CO和X2生成。已知反应中消耗1mol乙,可生成1.5molCO和1.5molX2。写出反应的化学方程式: ,氧化剂为 。
(12分)原子序数由小到大排列的X、Y、Z三种短周期元素,已知三种元素的原子序数之和等于16,单质X2 、Y2 、Z2之间有如下转化关系(反应条件已略)。已知:甲、乙分子中均含有10个电子;丙分子中含有15个电子。请回答: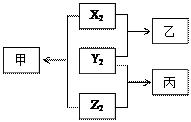
(1)Y2的电子式是___ ______;该分子中有 个σ键, 个π键。
(2)甲属于(填“极性”或“非极性”) 分子;晶体中甲分子的配位数为  。
。
(3)乙分子的VSEPR模型名称为 ,分子的立体构型名称为 。
(4)写出乙与Z2反应生成丙的化学方程式 。
(5)工业上用氧化铝、碳和乙在1400℃条件下反应,制取由元素Y和Al组成的化合物丁,同时还有CO和X2生成。已知反应中消耗1mol乙,可生成1.5molCO和1.5molX2。写出反应的化学方程式: ,氧化剂为 。
(12分)构成物质的微粒很多,离子就是构成物质的基本微粒之一,下表是中学化学中常见的几种离子:
回答下列问题:
(1)K+离子的结构示意图 ,Cl在周期表中的位置是 。
(2)将含OH-离子的溶液滴入浓度为0.1mol/L的Al3+和NH+4的混合溶液中,若测得溶液中NH+4减少了一半,则此时溶液中 (填“存在”或“不存在”)大量的Al3+。
(3)物质A和B分别由上表中的两种离子组成,将它们分别溶于水中,A的溶液显酸性,B的溶液显碱性且B的焰色反应呈紫色(透过蓝色钻玻璃观察),将A、B两溶液混合,既有白色沉淀生成,又有无色无味的气体生成。则A中含有的阳离子是 ,B溶液显碱性的原因是(用离子方程式和必要的文字说明) 。
(4)常温下,将(NH4)2CO3溶于水,得到含有大量NH4+和CO2-3的溶液,往溶液中滴入少量氨水,测得溶液中NH+4和CO2-3的浓度比为2:1,则此时该溶液的pH (填“<”、 “=”或“>”)7。
(5)在微生物作用下的条件,NH+4可被空气氧化成NO-3。写出该反应的离子方程式
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com