
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
вбжЊЃК
Ђй![]()
![]()
Ђк![]()
![]()
ЯТСае§ШЗЕФбЁЯюЪЧ
AЃЎ![]()
![]()
BЃЎ![]()
![]()
CЃЎ![]()
![]()
DЃЎ![]()
![]()
|
вбжЊЃК ЂйCH4(g)ЃЋ4NO2(g)ЃН4NO(g)ЃЋCO2(g)ЃЋ2H2O(g)ЁЁІЄHЃНЃ574 kJЁЄmolЃ1 ЂкCH4(g)ЃЋ4NO(g)ЃН2N2(g)ЃЋCO2(g)ЃЋ2H2O(g)ЁЁІЄHЃНЃ1160 kJЁЄmolвЛ1ЃЎ ЯТСае§ШЗЕФбЁЯюЪЧ | |
| [ЁЁЁЁ] | |
AЃЎ |
CH4(g)ЃЋ2NO2(g)ЃНN2(g)ЃЋCO2(g)ЃЋ2H2O(l)ЁЁІЄHЃНЃ867 kJЁЄmolЃ1 |
BЃЎ |
CH4(g)ЃЋ2NO2(g)ЃНN2(g)ЃЋCO2(g)ЃЋ2H2O(g)ЁЁІЄHЃНЃ867 kJЁЄmolЃ1 |
CЃЎ |
CH4(g)ЃЋ2NO2(g)ЃНN2(g)ЃЋCO2(g)ЃЋ2H2O(g)ЁЁІЄHЃНЃ586 kJЁЄmolЃ1 |
DЃЎ |
CH4(g)ЃЋ2NO2(g)ЃНN2(g)ЃЋCO2(g)ЃЋ2H2O(g)ЁЁІЄHЃНЃЋ586 kJЁЄmolЃ1 |
вбжЊA(g)+B(g) 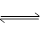 C(g)+D(g)ЗДгІЕФЦНКтГЃЪ§КЭЮТЖШЕФЙиЯЕШчЯТЃК
C(g)+D(g)ЗДгІЕФЦНКтГЃЪ§КЭЮТЖШЕФЙиЯЕШчЯТЃК
|
ЮТЖШ/ Ёц |
700 |
800 |
830 |
1000 |
1200 |
|
ЦНКтГЃЪ§ |
1.7 |
1.1 |
1.0 |
0.6 |
0.4 |
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉИУЗДгІЕФЦНКтГЃЪ§БэДяЪНK= ЃЌЁїH 0ЃЈЬюЁА<ЁБЁА >ЁБЁА =ЁБ)ЃЛ
ЃЈ2ЃЉ830ЁцЪБЃЌЯђвЛИі5 LЕФУмБеШнЦїжаГфШы0.20molЕФAКЭ0.80molЕФBЃЌШчЗДгІГѕЪМ6sФкAЕФЦНОљЗДгІЫйТЪv(A)=0.003 molЁЄL-1ЁЄs-1ЃЌдђ6sЪБc(A)= molЁЄL-1ЃЌ CЕФЮяжЪЕФСПЮЊ molЃЛШєЗДгІОвЛЖЮЪБМфКѓЃЌДяЕНЦНКтЪБAЕФзЊЛЏТЪЮЊ ЃЌШчЙћетЪБЯђИУУмБеШнЦїжадйГфШы1 molыВЦјЃЌЦНКтЪБAЕФзЊЛЏТЪЮЊ ЃЛ
ЃЈ3ЃЉХаЖЯИУЗДгІЪЧЗёДяЕНЦНКтЕФвРОнЮЊ (Ьюе§ШЗбЁЯюЧАЕФзжФИ)ЃК
aЃЎбЙЧПВЛЫцЪБМфИФБф bЃЎЦјЬхЕФУмЖШВЛЫцЪБМфИФБф
cЃЎc(A)ВЛЫцЪБЮЪИФБф dЃЎЕЅЮЛЪБМфРяЩњГЩCКЭDЕФЮяжЪЕФСПЯрЕШ
ЃЈ4ЃЉ1200ЁцЪБЗДгІC(g)+D(g) A(g)+B(g)ЕФЦНКтГЃЪ§ЕФжЕЮЊ
ЁЃ
A(g)+B(g)ЕФЦНКтГЃЪ§ЕФжЕЮЊ
ЁЃ
вбжЊA(g)+B(g)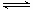 2 C(g)ЗДгІЕФЦНКтГЃЪ§КЭЮТЖШЕФЙиЯЕШчЯТЃК
2 C(g)ЗДгІЕФЦНКтГЃЪ§КЭЮТЖШЕФЙиЯЕШчЯТЃК
| ЮТЖШ/ Ёц | 700 | 800 | 830 | 1000 | 1200 |
| ЦНКтГЃЪ§ | 1ЃЎ70 | 1ЃЎ10 | 1ЃЎ00 | 0ЃЎ60 | 0ЃЎ40 |
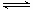 A(g)+B(g)ЕФЦНКтГЃЪ§ЕФжЕЮЊ ЁЃ
A(g)+B(g)ЕФЦНКтГЃЪ§ЕФжЕЮЊ ЁЃЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com