ЁАЮТЪваЇгІЁБЪЧИчБОЙўИљЦјКђБфЛЏДѓЛсбаОПЕФЛЗОГЮЪЬтжЎвЛЁЃCO2ЪЧФПЧАДѓЦјжаКЌСПзюИпЕФвЛжжЮТЪвЦјЬхЁЃвђДЫЃЌПижЦКЭжЮРэCO2ЪЧНтОіЁАЮТЪваЇгІЁБЕФгааЇЭООЖЁЃ
ЃЈ1ЃЉ ЦфжавЛжжЭООЖЪЧНЋCO2зЊЛЏГЩгаЛњЮяЪЕЯжЬМбЛЗЁЃШчЃК
2CO2(g)ЃЋ2H2O(l) == C2H4(g)ЃЋ3O2(g) ІЄHЃН+1411.0 kJ/mol
2CO2(g)ЃЋ3H2O(l) == C2H5OH(1)ЃЋ3O2(g) ІЄHЃН+1366.8 kJ/mol
дђгЩввЯЉЫЎЛЏжЦввДМЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊ ЁЃ
ЃЈ2ЃЉдквЛЖЈЬѕМўЯТЃЌ6H2(g) +2CO2(g)  CH3CH2OH(g)+3H2O(g)ЁЃ
CH3CH2OH(g)+3H2O(g)ЁЃ
| | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
ИљОнЩЯБэжаЪ§ОнЗжЮіЃК
Ђй ЮТЖШвЛЖЈЪБЃЌЬсИпЧтЬМБШ[n(H2)/n(CO2)]ЃЌCO2ЕФзЊЛЏТЪ ЃЈЬюЁАдіДѓЁБЁАМѕаЁЁБЁАВЛБфЁБЃЉЁЃ
Ђк ИУЗДгІЕФе§ЗДгІЮЊ ЃЈЬюЁАЮќЁБЛђЁАЗХЁБЃЉШШЗДгІЁЃ
ЃЈ3ЃЉвЛЖЈЬѕМўЯТЃЌНЋ3molH2КЭ1molCO2СНжжЦјЬхЛьКЯгкЙЬЖЈШнЛ§ЮЊ2LЕФУмБеШнЦїжаЃЌЗЂЩњШчЯТЗДгІЃК3H2ЃЈgЃЉ+ CO2ЃЈgЃЉ CH3OHЃЈgЃЉ+ H2OЃЈgЃЉЁЃ2minФЉИУЗДгІДяЕНЦНКтЃЌВтЕУCH3OHЕФХЈЖШЮЊ0.2mol/LЁЃЯТСаХаЖЯВЛе§ШЗЕФЪЧ ЁЃ
CH3OHЃЈgЃЉ+ H2OЃЈgЃЉЁЃ2minФЉИУЗДгІДяЕНЦНКтЃЌВтЕУCH3OHЕФХЈЖШЮЊ0.2mol/LЁЃЯТСаХаЖЯВЛе§ШЗЕФЪЧ ЁЃ
a. ИУЬѕМўЯТДЫЗДгІЕФЛЏбЇЦНКтГЃЪ§БэДяЪНЮЊ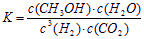
b. H2ЕФЦНОљЗДгІЫйТЪЮЊ0ЃЎ3mol/(LЁЄs)
c. CO2ЕФзЊЛЏТЪЮЊ60%
d. ШєЛьКЯЦјЬхЕФУмЖШВЛдйИФБфЪБЃЌИУЗДгІвЛЖЈДяЕНЦНКтзДЬЌ
|
ВщПДД№АИКЭНтЮі>>
ЁАЮТЪваЇгІЁБЪЧИчБОЙўИљЦјКђБфЛЏДѓЛсбаОПЕФЛЗОГЮЪЬтжЎвЛЁЃCO2ЪЧФПЧАДѓЦјжаКЌСПзюИпЕФвЛжжЮТЪвЦјЬхЁЃвђДЫЃЌПижЦКЭжЮРэCO2ЪЧНтОіЁАЮТЪваЇгІЁБЕФгааЇЭООЖЁЃ ЃЈ1ЃЉ ЦфжавЛжжЭООЖЪЧНЋCO2зЊЛЏГЩгаЛњЮяЪЕЯжЬМбЛЗЁЃШчЃК 2CO2(g)ЃЋ2H2O(l) == C2H4(g)ЃЋ3O2(g) ІЄHЃН+1411.0 kJ/mol 2CO2(g)ЃЋ3H2O(l) == C2H5OH(1)ЃЋ3O2(g) ІЄHЃН+1366.8 kJ/mol дђгЩввЯЉЫЎЛЏжЦввДМЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊ ЁЃ ЃЈ2ЃЉдквЛЖЈЬѕМўЯТЃЌ6H2(g) +2CO2(g)  CH3CH2OH(g)+3H2O(g)ЁЃ CH3CH2OH(g)+3H2O(g)ЁЃ | | 500 | 600 | 700 | 800 | | 1.5 | 45 | 33 | 20 | 12 | | 2 | 60 | 43 | 28 | 15 | | 3 | 83 | 62 | 37 | 22 | ИљОнЩЯБэжаЪ§ОнЗжЮіЃК Ђй ЮТЖШвЛЖЈЪБЃЌЬсИпЧтЬМБШ[n(H2)/n(CO2)]ЃЌCO2ЕФзЊЛЏТЪ ЃЈЬюЁАдіДѓЁБЁАМѕаЁЁБЁАВЛБфЁБЃЉЁЃ Ђк ИУЗДгІЕФе§ЗДгІЮЊ ЃЈЬюЁАЮќЁБЛђЁАЗХЁБЃЉШШЗДгІЁЃ ЃЈ3ЃЉвЛЖЈЬѕМўЯТЃЌНЋ3molH2КЭ1molCO2СНжжЦјЬхЛьКЯгкЙЬЖЈШнЛ§ЮЊ2LЕФУмБеШнЦїжаЃЌЗЂЩњШчЯТЗДгІЃК3H2ЃЈgЃЉ+ CO2ЃЈgЃЉ CH3OHЃЈgЃЉ+ H2OЃЈgЃЉЁЃ2minФЉИУЗДгІДяЕНЦНКтЃЌВтЕУCH3OHЕФХЈЖШЮЊ0.2mol/LЁЃЯТСаХаЖЯВЛе§ШЗЕФЪЧ ЁЃ CH3OHЃЈgЃЉ+ H2OЃЈgЃЉЁЃ2minФЉИУЗДгІДяЕНЦНКтЃЌВтЕУCH3OHЕФХЈЖШЮЊ0.2mol/LЁЃЯТСаХаЖЯВЛе§ШЗЕФЪЧ ЁЃ a. ИУЬѕМўЯТДЫЗДгІЕФЛЏбЇЦНКтГЃЪ§БэДяЪНЮЊ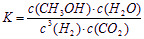 b. H2ЕФЦНОљЗДгІЫйТЪЮЊ0ЃЎ3mol/(LЁЄs) c. CO2ЕФзЊЛЏТЪЮЊ60% d. ШєЛьКЯЦјЬхЕФУмЖШВЛдйИФБфЪБЃЌИУЗДгІвЛЖЈДяЕНЦНКтзДЬЌ |
ВщПДД№АИКЭНтЮі>>
дквЛЙЬЖЈШнЛ§ЕФУмБеШнЦїжаЃЌНјааШчЯТЗДгІЃК
C(s)ЃЋH2O(g) CO(g)ЃЋH2(g) CO(g)ЃЋH2(g)
27.ЗДгІКѓЮяжЪЕФзмФмСПдіДѓЃЌдђИУЗДгІЮЊ________ЗДгІ(ЬюЁАЮќШШЁБЛђЁАЗХШШЁБ)ЁЃ
28.ВЛФмХаЖЯИУЗДгІЪЧЗёДяЕНЛЏбЇЦНКтзДЬЌЕФЪЧ________ЃЈбЁЬюБрКХЃЉЁЃ
aЃЎШнЦїжаЦјЬхбЙЧПВЛБф bЃЎЛьКЯЦјЬхжаc(CO)ВЛБф
cЃЎvе§(H2)ЃНvФц(H2O) dЃЎc(H2O)ЃНc(CO)
29.ШєШнЦїШнЛ§ЮЊ2LЃЌЗДгІ10sКѓВтЕУЛьКЯЦјЬхЕФзмжЪСПдіМгСЫ2.4g, дђCOЕФЦНОљЗДгІЫйТЪЮЊ mol/(L?S)ЃЛШєдйдіМгЙЬЬЌЬМЕФСПЃЌдђе§ЗДгІЕФЫйТЪ ЃЈбЁЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЁЂЁАВЛБфЁБЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
дквЛЙЬЖЈШнЛ§ЕФУмБеШнЦїжаЃЌНјааШчЯТЗДгІЃК C(s)ЃЋH2O(g) CO(g)ЃЋH2(g) CO(g)ЃЋH2(g) 27.ЗДгІКѓЮяжЪЕФзмФмСПдіДѓЃЌдђИУЗДгІЮЊ________ЗДгІ(ЬюЁАЮќШШЁБЛђЁАЗХШШЁБ)ЁЃ 28.ВЛФмХаЖЯИУЗДгІЪЧЗёДяЕНЛЏбЇЦНКтзДЬЌЕФЪЧ________ЃЈбЁЬюБрКХЃЉЁЃ aЃЎШнЦїжаЦјЬхбЙЧПВЛБф bЃЎЛьКЯЦјЬхжаc(CO)ВЛБф cЃЎvе§(H2)ЃНvФц(H2O) dЃЎc(H2O)ЃНc(CO) 29.ШєШнЦїШнЛ§ЮЊ2LЃЌЗДгІ10sКѓВтЕУЛьКЯЦјЬхЕФзмжЪСПдіМгСЫ2.4g, дђCOЕФЦНОљЗДгІЫйТЪЮЊ mol/(L?S)ЃЛШєдйдіМгЙЬЬЌЬМЕФСПЃЌдђе§ЗДгІЕФЫйТЪ ЃЈбЁЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЁЂЁАВЛБфЁБЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
дквЛЙЬЖЈШнЛ§ЕФУмБеШнЦїжаЃЌНјааШчЯТЗДгІЃК C(s)ЃЋH 2O(g)  CO(g)ЃЋH 2(g) 27.ЗДгІКѓЮяжЪЕФзмФмСПдіДѓЃЌдђИУЗДгІЮЊ________ЗДгІ(ЬюЁАЮќШШЁБЛђЁАЗХШШЁБ)ЁЃ 28.ВЛФмХаЖЯИУЗДгІЪЧЗёДяЕНЛЏбЇЦНКтзДЬЌЕФЪЧ________ЃЈбЁЬюБрКХЃЉЁЃ aЃЎШнЦїжаЦјЬхбЙЧПВЛБф bЃЎЛьКЯЦјЬхжаc(CO)ВЛБф cЃЎv е§(H 2)ЃНv Фц(H 2O) dЃЎc(H 2O)ЃНc(CO) 29.ШєШнЦїШнЛ§ЮЊ2LЃЌЗДгІ10sКѓВтЕУЛьКЯЦјЬхЕФзмжЪСПдіМгСЫ2.4g, дђCOЕФЦНОљЗДгІЫйТЪЮЊ mol/(L?S)ЃЛШєдйдіМгЙЬЬЌЬМЕФСПЃЌдђе§ЗДгІЕФЫйТЪ ЃЈбЁЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЁЂЁАВЛБфЁБЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
| | | |

![]() CH3CH2OH(g)+3H2O(g)ЁЃ
CH3CH2OH(g)+3H2O(g)ЁЃ ![]() CH3OHЃЈgЃЉ+ H2OЃЈgЃЉЁЃ2minФЉИУЗДгІДяЕНЦНКтЃЌВтЕУCH3OHЕФХЈЖШЮЊ0.2mol/LЁЃЯТСаХаЖЯВЛе§ШЗЕФЪЧ ЁЃ
CH3OHЃЈgЃЉ+ H2OЃЈgЃЉЁЃ2minФЉИУЗДгІДяЕНЦНКтЃЌВтЕУCH3OHЕФХЈЖШЮЊ0.2mol/LЁЃЯТСаХаЖЯВЛе§ШЗЕФЪЧ ЁЃ![]()