
题目列表(包括答案和解析)
氯化钠、氢氧化钠 、碳酸钠和碳酸氢钠是生活中常见的物质。
请回答下列问题。
(1)粗盐中含有可溶性CaCl2、MgCl2 Na2SO4杂质,除去这些杂质的试剂可选用
①Na2CO3、②NaOH、③BaCl2、④ HCl ,加入试剂的先后顺序可以是
(2)等质量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者 后者
(填 >、< 或 =)。
(3)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为
。
(4) 除去NaHCO3溶液中的少量Na2CO3,方法是:
离子方程式: 。
(5)钠与氢气在加热条件下能发生反应,生成一种白色固体。其中氢元素的化合价为-1价,写出白色固体与水剧烈反应生成氢气的化学方程式为
(1).
下列有关电化学的图示中,完全正确的是________
(2).
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中可与碘化物作用生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.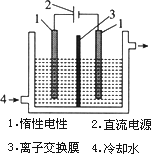
请回答下列问题:
a.碘是________(填颜色)固体物质,实验室常用________方法来分离提纯含有少量泥沙杂质的固体碘.
b.电解前,先将一定量的精制碘溶于过量氢氧化钾溶液,溶解时发生反应:3I2+6KOH![]() 5KI+KIO3+3H2O,将该溶液加入阳极区.另将氢氧化钾溶液加入阴极区,电解槽用水冷却.
5KI+KIO3+3H2O,将该溶液加入阳极区.另将氢氧化钾溶液加入阴极区,电解槽用水冷却.
电解时,阳极上发生反应的电极反应式为________,每生成1 mol KIO3,电路中通过的电子的物质的量为________.
c.电解过程中,为确定电解是否完成,需检验电解液中是否有I-.请设计一个检验电解液中是否有I-的简单实验方案,并按要求填写下表.
![]()
可供选择的试剂有淀粉溶液,稀硫酸,氯化钠溶液,酒精等.(用其中的一种或多种均可.)
d.电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
阳极电解液→①蒸发浓缩→②→③过滤→④洗涤→⑤→碘酸钾晶体
步骤②的操作名称是________,步骤⑤的操作名称是________.步骤④洗涤晶体的目的是________.
(12分)(1).下列有关电化学的图示中,完全正确的是
(2).碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中可与碘化物作用生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如图所示。
请回答下列问题:
a、碘是 (填颜色)固体物质,实验室常用 方法来分离提纯含有少量泥沙杂质的固体碘。
b、电解前,先将一定量的精制碘溶于过量氢氧化钾溶
液,溶解时发生反应:3I2+6KOH==5KI+KIO3+3H2O,
将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为 ,每生成1mol KIO3,电路中通过的电子的物质的量为___________________。
c、电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验
电解液中是否有I-的简单实验方案,并按要求填写下表。
可供选择的试剂有淀粉溶液,稀硫酸,氯化钠溶液,酒精等。(用其中的一种或多种均可。)
| 实验方法 | 实验现象及结论 |
|
|
|
d、电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:
阳极电解液→①蒸发浓缩→②→③过滤→④洗涤→⑤→碘酸钾晶体
步骤②的操作名称是 ,步骤⑤的操作名称是 。步骤④洗涤
晶体的目的是 。
(12分)(1).下列有关电化学的图示中,完全正确的是 
(2).碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中可与碘化物作用生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如图所示。
请回答下列问题:
a、碘是 (填颜色)固体物质,实验室常用 方法来分离提纯含有少量泥沙杂质的固体碘。
b、电解前,先将一定量的精制碘溶于过量氢氧化钾溶
液,溶解时发生反应:3I2+6KOH==5KI+KIO3+3H2O,
将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为 ,每生成1mol KIO3,电路中通过的电子的物质的量为___________________。
c、电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验
电解液中是否有I-的简单实验方案,并按要求填写下表。
可供选择的试剂有淀粉溶液,稀硫酸,氯化钠溶液,酒精等。(用其中的一种或多种均可。)
| 实验方法 | 实验现象及结论 |
| | |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com