
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
(1)¼×µÄ»ÆѧŹ½ĪŖRClx”£
¢ŁČō¼×ĪŖij¶ĢÖÜĘŚ½šŹōŌŖĖŲµÄĀČ»ÆĪļ£¬¼×ÖŠŗ¬ÓŠµÄ½šŹōŌŖĖŲµÄŌ×Ó°ė¾¶ŌŚĶ¬ÖÜĘŚ½šŹōŌŖĖŲÖŠ×īŠ”£¬ĘäŃōĄė×ÓÓėÄŹŌ×ÓÓŠĻąĶ¬µÄµē×Ó²ć½į¹¹”£Ōņ¼×ÖŠŗ¬ÓŠµÄ½šŹōŌŖĖŲŹĒ________£»
¢ŚČō¼×ĪŖij½šŹōŌŖĖŲµÄ×ŲÉ«ĀČ»ÆĪļ£¬½«øĆĀČ»ÆĪļĖ®ČÜŅŗ¼ÓČČÕōøɲ¢×ĘÉÕ£¬µĆµ½µÄŃõ»ÆĪļĪŖŗģ×ŲÉ«·ŪÄ©£¬Ōņ¼×µÄ»ÆѧŹ½ĪŖ________£¬¼×ÖŠŗ¬ÓŠµÄ½šŹōŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖ________£¬
¢Ū½«ÉĻŹöĮ½ÖÖ½šŹōÖŠ»īĘĆŠŌĒæµÄ½šŹōÓėĮķŅ»ÖÖ½šŹōµÄ×īøß¼ŪŃõ»ÆĪļ»ģŗĻ£¬ŅżČ¼ŗóæÉ·¢Éś¾ēĮŅ·“Ó¦£¬Ęä»Æѧ·½³ĢŹ½ĪŖ________£¬ŅżČ¼øĆ·“Ó¦µÄŹµŃé²Ł×÷ŹĒ________”£
(2)Čō¼×”¢ŅŅ”¢±ū”¢¶”ĪŖµ„ÖŹ»ņ»ÆŗĻĪļ£¬¾łŗ¬ÓŠÄ³¶ĢÖÜĘŚÖŠµÄĶ¬Ņ»ÖÖŌŖĖŲ£¬³£ĪĀĻĀ¼×ĪŖĘųĢ壬½«¼×ĶØČė³£ĪĀĻĀµÄKOHČÜŅŗÖŠµĆµ½ŅŅŗĶ±ū£¬±ūµÄĖ®ČÜŅŗ¾ßÓŠĒæŃõ»ÆŠŌ”£
¢Łµē½āŅŅČÜŅŗµĆµ½¼×£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ__________£»
¢ŚŌŚŅ»¶ØĢõ¼žĻĀ1 mol¼×Óė2 mol KOHŌŚČÜŅŗÖŠ·“Ó¦µĆµ½ŅŅŗĶ¶”£¬n(ŅŅ)£ŗn(¶”)=5:1£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ___________________”£
£Ø13·Ö£©ŅŃÖŖ¼×”¢ŅŅ”¢±ū·Ö±š“ś±ķ֊ѧ»Æѧ֊µÄ³£¼ūĪļÖŹ£¬Ēėøł¾ŻĢāÄæŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Čō¼×µÄ»ÆѧŹ½ĪŖRCl3£¬ĘäČÜŅŗŌŚ¼ÓČČÕōÓŚ²¢×ĘÉÕŹ±æÉ·¢ÉśČēĻĀ·“Ó¦£ŗ
a£®¼×+H2O![]() ŅŅŹ®±ū b£®ŅŅ
ŅŅŹ®±ū b£®ŅŅ![]() Ńõ»ÆĪļ+H2O
Ńõ»ÆĪļ+H2O
¢ŁČō¼×ĪŖijÓĆĶ¾¹ć·ŗµÄ½šŹōŌŖĖŲµÄĀČ»ÆĪļ£¬ĘäČÜŅŗŌŚÉĻŹö±ä»ÆÖŠÉś³ÉµÄŃõ»ÆĪļĪŖŗģ×ŲÉ«·ŪÄ©£¬ŌņøĆ½šŹōŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ£ŗ ”£
¢ŚČō¼×ĪŖij¶ĢÖÜĘŚ½šŹōŌŖĖŲµÄĀČ»ÆĪļ£¬Ōņ¼×·¢Éśa·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ____”£
¢Ū½«ŅŌÉĻĮ½ÖÖ½šŹōµ„ÖŹÓƵ¼ĻßĮ¬½Ó£¬²åČėŅ»øöŹ¢ÓŠNaOHČÜŅŗµÄÉÕ±ÖŠ¹¹³ÉŌµē³Ų£¬Ōņøŗ¼«·¢ÉśµÄµē¼«·“Ó¦ĪŖ ”£
£Ø2£©Čō¼×”¢ŅŅ”¢±ū¾łŹĒ¶ĢÖÜĘŚÖŠĶ¬Ņ»ÖÜĘŚŌŖĖŲŠĪ³ÉµÄµ„ÖŹ»ņ»ÆŗĻĪļ£¬³£ĪĀĻĀŅŅĪŖ¹ĢĢåµ„ÖŹ£¬¼×ŗĶ±ū¾łĪŖĘųĢ¬»ÆŗĻĪļ£¬ĒŅæÉ·¢Éś·“Ó¦£ŗ¼×Ź®ŅŅ![]() ±ū”£Ōņ£ŗ
±ū”£Ōņ£ŗ
¢Ł¼×µÄ½į¹¹Ź½ĪŖ ”£
¢ŚŠ“³öÉĻŹö·“Ó¦µÄ»Æѧ·½³ĢŹ½ ”£
¢ŪŠ“³öŌŚ200mL 2mol£ÆLµÄNaOHČÜŅŗÖŠĶØČė6.72L£Ø±ź×¼×“æö£©µÄĘųĢå¼×·¢ÉśĶźČ«·“Ó¦µÄ×ÜĄė×Ó·½³ĢŹ½ ”£
£Ø13·Ö£©ŅŃÖŖ¼×”¢ŅŅ”¢±ū·Ö±š“ś±ķ֊ѧ»Æѧ֊µÄ³£¼ūĪļÖŹ£¬Ēėøł¾ŻĢāÄæŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Čō¼×µÄ»ÆѧŹ½ĪŖRCl3£¬ĘäČÜŅŗŌŚ¼ÓČČÕōÓŚ²¢×ĘÉÕŹ±æÉ·¢ÉśČēĻĀ·“Ó¦£ŗ
a£®¼×+H2O ŅŅŹ®±ū b£®ŅŅ
ŅŅŹ®±ū b£®ŅŅ Ńõ»ÆĪļ+H2O
Ńõ»ÆĪļ+H2O
¢ŁČō¼×ĪŖijÓĆĶ¾¹ć·ŗµÄ½šŹōŌŖĖŲµÄĀČ»ÆĪļ£¬ĘäČÜŅŗŌŚÉĻŹö±ä»ÆÖŠÉś³ÉµÄŃõ»ÆĪļĪŖŗģ×ŲÉ«·ŪÄ©£¬ŌņøĆ½šŹōŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ£ŗ ”£
¢ŚČō¼×ĪŖij¶ĢÖÜĘŚ½šŹōŌŖĖŲµÄĀČ»ÆĪļ£¬Ōņ¼×·¢Éśa·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ____”£
¢Ū½«ŅŌÉĻĮ½ÖÖ½šŹōµ„ÖŹÓƵ¼ĻßĮ¬½Ó£¬²åČėŅ»øöŹ¢ÓŠNaOHČÜŅŗµÄÉÕ±ÖŠ¹¹³ÉŌµē³Ų£¬Ōņøŗ¼«·¢ÉśµÄµē¼«·“Ó¦ĪŖ ”£
£Ø2£©Čō¼×”¢ŅŅ”¢±ū¾łŹĒ¶ĢÖÜĘŚÖŠĶ¬Ņ»ÖÜĘŚŌŖĖŲŠĪ³ÉµÄµ„ÖŹ»ņ»ÆŗĻĪļ£¬³£ĪĀĻĀŅŅĪŖ¹ĢĢåµ„ÖŹ£¬¼×ŗĶ±ū¾łĪŖĘųĢ¬»ÆŗĻĪļ£¬ĒŅæÉ·¢Éś·“Ó¦£ŗ¼×Ź®ŅŅ ±ū”£Ōņ£ŗ
±ū”£Ōņ£ŗ
¢Ł¼×µÄ½į¹¹Ź½ĪŖ ”£
¢ŚŠ“³öÉĻŹö·“Ó¦µÄ»Æѧ·½³ĢŹ½ ”£
¢ŪŠ“³öŌŚ200mL 2mol£ÆLµÄNaOHČÜŅŗÖŠĶØČė6.72L£Ø±ź×¼×“æö£©µÄĘųĢå¼×·¢ÉśĶźČ«·“Ó¦µÄ×ÜĄė×Ó·½³ĢŹ½ ”£
ŅŃÖŖ¼×”¢ŅŅ”¢±ū·Ö±š“ś±ķ֊ѧ»Æѧ֊µÄ³£¼ūĪļÖŹ£¬Ēėøł¾ŻĢāÄæŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ń£®Čō¼×µÄ»ÆѧŹ½ĪŖRCl3£¬ĘäČÜŅŗŌŚ¼ÓČČÕōøɲ¢×ĘÉÕŹ±æÉ·¢Éś·“Ó¦£ŗ
a.¼×+H2O ŅŅ+±ū b.ŅŅ
ŅŅ+±ū b.ŅŅ Ńõ»ÆĪļ+H2O
Ńõ»ÆĪļ+H2O
¢ŁČō¼×ĪŖijÓĆĶ¾¹ć·ŗµÄ½šŹōŌŖĖŲµÄĀČ»ÆĪļ£¬ĘäČÜŅŗŌŚÉĻŹö±ä»ÆÖŠÉś³ÉµÄŃõ»ÆĪļĪŖŗģ×ŲÉ«·ŪÄ©£¬Ōņ¼×·¢Éśa·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ
¢ŚČō¼×ĪŖij¶ĢÖÜĘŚ½šŹōŌŖĖŲµÄĀČ»ÆĪļ£¬ŌņøĆ½šŹōŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ£ŗ £»
ČōĻņ30 mL 1 mol/LµÄ¼×µÄČÜŅŗÖŠÖš½„¼ÓČėÅضČĪŖ4 mol/LµÄNaOHČÜŅŗ£¬Čō²śÉś0.78 g°×É«³Įµķ£¬Ōņ¼ÓČėµÄNaOHČÜŅŗµÄĢå»żæÉÄÜĪŖ £ØŃ”Ģī±ąŗÅ£©.
| A£®3 mL | B£®7.5 mL | C£®15 mL | D£®27.5 mL |
 ±ū”£Ōņ£ŗ
±ū”£Ōņ£ŗ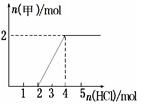
ŅŃÖŖ¼×”¢ŅŅ”¢±ū·Ö±š“ś±ķ֊ѧ»Æѧ֊µÄ³£¼ūĪļÖŹ£¬Ēėøł¾ŻĢāÄæŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Čō¼×µÄ»ÆѧŹ½ĪŖRCl3£¬ĘäČÜŅŗŌŚ¼ÓČČÕōøɲ¢×ĘÉÕŹ±æÉ·¢Éś·“Ó¦£ŗ
a£®¼×+H2O![]() ŅŅ+±ū b£®ŅŅ
ŅŅ+±ū b£®ŅŅ![]() Ńõ»ÆĪļ+H2O
Ńõ»ÆĪļ+H2O
¢ŁČō¼×ĪŖijÓĆĶ¾¹ć·ŗµÄ½šŹōŌŖĖŲµÄĀČ»ÆĪļ£¬ĘäČÜŅŗŌŚÉĻŹö±ä»ÆÖŠÉś³ÉµÄŃõ»ÆĪļĪŖŗģ
×ŲÉ«·ŪÄ©£¬ŌņøĆ½šŹōŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒ ”£
¢ŚČō¼×ĪŖij¶ĢÖÜĘŚ½šŹōŌŖĖŲµÄĀČ»ÆĪļ£¬Ōņ¼×·¢Éśa·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ
_ ӣ
¢Ū½«ŅŌÉĻĮ½ÖÖ½šŹōµ„ÖŹÓƵ¼ĻßĮ¬½Ó£¬²åČėŅ»øöŹ¢ÓŠNaOHČÜŅŗµÄÉÕ±ÖŠ¹¹³ÉŌµē³Ų£¬
Ōņøŗ¼«·¢ÉśµÄµē¼«·“Ó¦ĪŖ ”£
£Ø2£©Čō¼×£¬ŅŅ”¢±ū¾łŹĒ¶ĢÖÜĘŚÖŠĶ¬Ņ»ÖÜĘŚŌŖĖŲŠĪ³ÉµÄµ„ÖŹ»ņ»ÆŗĻĪļ£¬³£ĪĀĻĀŅŅĪŖ¹ĢĢ嵄
ÖŹ£¬¼×ŗĶ±ū¾łĪŖĘųĢ¬»ÆŗĻĪļ£¬ĒŅæÉ·¢Éś·“Ó¦£ŗ¼×+ŅŅ![]() ±ū”£
±ū”£
Ōņ£ŗ¢Ł¼×µÄ½į¹¹Ź½ĪŖ ”£
¢ŚŠ“³öÉĻŹö·“Ó¦µÄ»Æѧ·½³ĢŹ½ ”£
¢ŪŠ“³öŌŚ200mL 2mol£ÆLµÄNaOHČÜŅŗÖŠĶØČė6.72L(±ź×¼×“æö)µÄĘųĢå¼×·¢Éś
ĶźČ«·“Ó¦µÄ×ÜĄė×Ó·½³ĢŹ½ ”£
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com