
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
вбжЊ25 ЁцЪБШѕЕчНтжЪЕФЕчРыЦНКтГЃЪ§ЃК
Ka(CH3COOH)ЃН1.8ЁС10Ѓ5ЃЌKa(HSCN)ЃН0.13ЁЃ
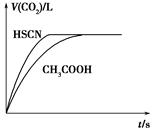
(1)НЋ20 mL 0.10 molЁЄLЃ1 CH3COOHШмвККЭ20 mL 0.10 molЁЄLЃ1ЕФHSCNШмвКЗжБ№гы0.10 molЁЄLЃ1ЕФNaHCO3ШмвКЗДгІЃЌЪЕбщВтЕУВњЩњCO2ЦјЬхЬхЛ§(V)гыЪБМфtЕФЙиЯЕШчЭМЫљЪОЁЃ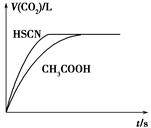
ЗДгІПЊЪМЪБЃЌСНжжШмвКВњЩњCO2ЕФЫйТЪУїЯдВЛЭЌЕФдвђЪЧ________ЃЛЗДгІНсЪјКѓЫљЕУШмвКжаc(SCNЃ)________c(CH3COOЃ)(ЬюЁАЃОЁБЁЂЁАЃНЁБЛђЃМ)ЁЃ
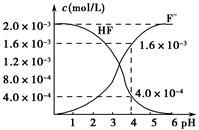
(2)2.0ЁС10Ѓ3 molЁЄLЃ1ЕФЧтЗњЫсЫЎШмвКжаЃЌЕїНкШмвКpH(КіТдЕїНкЪБЬхЛ§БфЛЏ)ЃЌВтЕУЦНКтЬхЯЕжаc(FЃ)ЁЂc(HF)гыШмвКpHЕФЙиЯЕШчЭМЫљЪОЁЃдђ25 ЁцЪБЃЌHFЕчРыЦНКтГЃЪ§ЮЊKa(HF)ЃН________(СаЪНЧѓжЕ)ЁЃ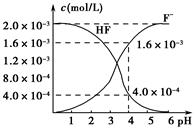
(3)ФбШмЮяжЪCaF2ШмЖШЛ§ГЃЪ§ЮЊKspЃН1.5ЁС10Ѓ10ЃЌНЋ4.0ЁС10Ѓ3 molЁЄLЃ1 HFШмвКгы4.0ЁС10Ѓ4 molЁЄLЃ1ЕФCaCl2ШмвКЕШЬхЛ§ЛьКЯЃЌЕїНкШмвКpHЃН4(КіТдЕїНкЪБШмвКЬхЛ§БфЛЏ)ЃЌЪдЗжЮіЛьКЯКѓЪЧЗёгаГСЕэЩњГЩЃП________(ЬюЁАгаЁБЛђЁАУЛгаЁБ)ЃЌМђЪіРэгЩЃК____________________________________________ЁЃ


(ДДаТдЄВтЬт)вбжЊ25 ЁцЪБШѕЕчНтжЪЕФЕчРыЦНКтГЃЪ§ЃК
Ka(CH3COOH)ЃН1.8ЁС10Ѓ5ЃЌKa(HSCN)ЃН0.13ЁЃ
(1)НЋ20 mL 0.10 molЁЄLЃ1 CH3COOHШмвККЭ20 mL 0.10 molЁЄLЃ1ЕФHSCNШмвКЗжБ№гы0.10 molЁЄLЃ1ЕФNaHCO3ШмвКЗДгІЃЌЪЕбщВтЕУВњЩњCO2ЦјЬхЬхЛ§(V)гы
ЪБМфtЕФЙиЯЕШчЭМЫљЪОЁЃ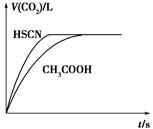
ЗДгІПЊЪМЪБЃЌСНжжШмвКВњЩњCO2ЕФЫйТЪУїЯдВЛЭЌЕФдвђЪЧ________ЃЛЗДгІНсЪјКѓЫљЕУШмвКжаc(SCNЃ)______c(CH3COOЃ)(ЬюЁАЃОЁБЁЂЁАЃНЁБЛђЃМ)ЁЃ
(2)2.0ЁС10Ѓ3 molЁЄLЃ1ЕФЧтЗњЫсЫЎШмвКжаЃЌЕїНкШмвКpH(КіТдЕїНкЪБЬхЛ§БфЛЏ)ЃЌВтЕУЦНКтЬхЯЕжаc(FЃ)ЁЂc(HF)гыШмвКpHЕФЙиЯЕШчЭМЫљЪОЁЃдђ25 ЁцЪБЃЌHFЕчРыЦНКтГЃЪ§ЮЊKa(HF)ЃН________(СаЪНЧѓжЕ)ЁЃ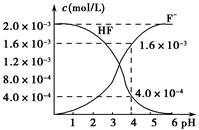
(3)ФбШмЮяжЪCaF2ШмЖШЛ§ГЃЪ§ЮЊKspЃН1.5ЁС10Ѓ10ЃЌНЋ4.0ЁС10Ѓ3 molЁЄLЃ1 HFШмвКгы4.0ЁС10Ѓ4 molЁЄLЃ1ЕФCaCl2ШмвКЕШЬхЛ§ЛьКЯЃЌЕїНкШмвКpHЃН4(КіТдЕїНкЪБШмвКЬхЛ§БфЛЏ)ЃЌЪдЗжЮіЛьКЯКѓЪЧЗёгаГСЕэЩњГЩЃП________(ЬюЁАгаЁБЛђЁАУЛгаЁБ)ЃЌМђЪіРэгЩЃК_____________________________________ЁЃ
 МзЁЂввСНзщЭЌбЇЗжБ№ЖдЭЁЂЬњгыЯѕЫсЕФЗДгІНјааЬНОПЃЌЧыФуВЮгыВЂЭъГЩЖдгаЙиЮЪЬтЕФНтД№ЃЎ
МзЁЂввСНзщЭЌбЇЗжБ№ЖдЭЁЂЬњгыЯѕЫсЕФЗДгІНјааЬНОПЃЌЧыФуВЮгыВЂЭъГЩЖдгаЙиЮЪЬтЕФНтД№ЃЎ| 11 |
| 3 |
| 11 |
| 3 |
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com