
题目列表(包括答案和解析)
|
用铅蓄电池作电源电解某溶液100 mL.已知该溶液中含SO2、KI,其物质的量浓度均为0.1 mol/L,如图所示(C1、C2为石墨电极),下列说法正确的是
| |
| [ ] | |
A. |
铅蓄电池工作一段时间后A溶液的pH变小 |
B. |
当B烧杯中I-的浓度降为0.05 mol/L时,消耗A中的H2SO4的物质的量为0.025 mol |
C. |
当C1、C2两极均产生气体时,应有至少3.6×1022个电子从电路中流过 |
D. |
铅蓄电池工作时负极电极反应式为:PbO2-2e-+H2SO4 |
|
用铅蓄电池作电源电解某溶液100 mL.已知该溶液中含KI和NaSO4,其物质的量的浓度均为0.1 mol/L,如图所示(C1、C2为石墨电极),下列说法正确的是
| |
| [ ] | |
A. |
电解一段时间后A溶液的pH变小 |
B. |
C1、C2两极产生的气体体积不可能相等 |
C. |
当C1、C2两极均产生气体时,至少由3.6×1022个电子从电路中流过 |
D. |
A池中负极电极反应式为:PbO2+2e-+2H2SO4 |
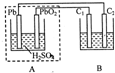
下图装置中,A为铅蓄电池,C1、C2为石墨电极,B烧杯中是浓度均为0.1mol/L的H2SO3和KI的混合溶液100mL。下列说法正确的是
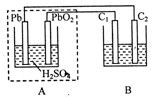
A.铅蓄电池工作一段时间后,A中溶液的PH变小
B.当B烧杯中I-的浓度降为0.05mol/L时,A中消耗的
H2SO3的物质的量为0.025mol
C.当C1、C2两极均开始产生气体时,至少已有3.6×1022个电子从电路中流过
D.铅蓄电池工作时,负极电极反应式为:PbO2-2e -+ H2SO3 = PbSO4+2H2O +SO42-
| A.铅蓄电池工作一段时间后,A中溶液的PH变小 |
| B.当B烧杯中I-的浓度降为0.05mol/L时,A中消耗的H2SO4的物质的量为0.025mol |
| C.当C1、C2两极均开始产生气体时,至少已有3.6×1022个电子从电路中流过 |
| D.铅蓄电池工作时,负极电极反应式为:PbO2-2e -+H2SO3=PbSO4+2H2O+SO42- |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com