A、J是日常生活中常见的两种金属,这两种金属和NaOH组成原电池,A作负极;F常温下是气体,各物质有以下的转化关系(部分产物及条件略去).

请回答以下问题:
(1)写出原电池的负极反应方程式
Al+4OH--3e-=AlO2-+2H2O
Al+4OH--3e-=AlO2-+2H2O
.
(2)常温时pH=12的C溶液中,溶质的阳离子与溶质的阴离子浓度之差为
10-2-10-12mol/L或c(OH-)-c(H+)
10-2-10-12mol/L或c(OH-)-c(H+)
(写出计算式);相同条件下,等浓度的C溶液与CH
3COONa溶液中,C的阴离子与CH
3COO
-浓度的大小关系:前者
<
<
后者(用“>”、“<”或“=”表示).
(3)金属A的氯化物沸点较低,又易升华,能否电解这种熔融氯化物来生产A?
否
否
.原因是
因为A的氯化物熔沸点低,据此判断它的晶体为分子晶体,在熔融态时不电离,不能被电解
因为A的氯化物熔沸点低,据此判断它的晶体为分子晶体,在熔融态时不电离,不能被电解
.
(4)写出A→J反应的化学方程式
.
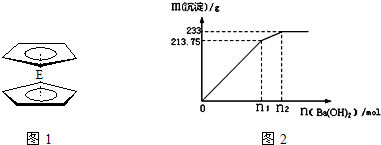
(5)由J制备的J(C
5H
5)
2的结构如图1,其中氢原子的化学环境完全相同.但早期人们却错误地认为它的结构为:

.核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有
1
1
种峰,错误的结构有
3
3
种峰.
(6)含A元素的某盐X常做净水剂,X做焰色反应时,透过钴玻璃观察火焰呈紫色.500mLX的溶液与Ba(OH)
2反应生成沉淀的质量
与加入Ba(OH)
2物质的量的关系如图2:请回答:X晶体的俗名为
明矾或白矾
明矾或白矾
;其溶液的物质量浓度为
1
1
mol/L.



 .核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有
.核磁共振法能够区分这两种结构.在核磁共振氢谱中,正确的结构有