
题目列表(包括答案和解析)
某白色晶体由碳、氢、氧三种元素组成,其中氢氧原子的个数比为2∶1,氢原子数比碳原子数多10,0.1mol的该物质经浓硫酸在低温下脱水后得干燥的焦炭14.4克,该物质的溶液与新制的氢氧化铜悬浊液共热无红色沉淀,此白色晶体的分子式是________,名称是________.
(12分)某活动小组探究某无色晶体(纯净物)的组成。先测得相对分子质量为126;经元素分析可知:只含碳、氢、氧三种元素;该无色晶体受热能分解。然后设计了下列实验方案再对其进行定量分析:
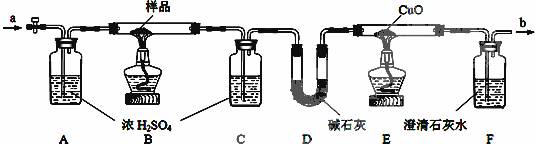
【实验操作】(1)检查装置的气密性;
(2)在相应的仪器中放入相应的试剂,并称量C、D、E的质量;
(3)先从a处通入足量的N2,排尽装置中的空气;
(4)点燃B、E两处的酒精灯,缓缓加热样品,使之发生分解反应;
(5)当样品完全分解后,先熄灭B处的酒精灯,从a处缓缓通入足量的N2,再熄灭E处酒精灯;
(6)冷至室温,拆下各仪器,并称量C、D、E的质量。
【实验现象】 ① E处有红色物质生成,F处有白色沉淀生成;
② 由于实验条件控制得好,b处无可燃性气体放出。
请回答下列问题:
(1)用最简便的方法检查整套装置的气密性:
。
(2)仪器A的作用是 。
(3)操作(3)和(5)若是通入空气,其后果是
。
(4)数据处理:
① 实验记录的数据(各仪器中的吸收或反应都很完全):
| 样品的质量 | C装置增重 | D装置增重 | E装置减轻 |
| 12.6 g | 5.4 g | 4.4 g | 1.6 g |
② 计算判断:样品(无色晶体)的分子式为______________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com