
题目列表(包括答案和解析)

| 浓硫酸 |
| 加热 |
| 浓硫酸 |
| 加热 |
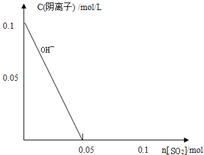
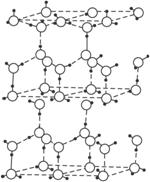
图2-13
(1)含1 mol冰中有___________mol“氢键”。
(2)水分子中可电离生成两种含有相同电子数的微粒,其电离方程式为___________。
(3)在冰的结构中,每个水分子与相邻的4个分子氢键相连接。在冰中除氢键外,还存在范德华力(11 kJ·mol-1)。已知冰的升华热是51 kJ·mol-1,则冰中氢键的能量是__________kJ·mol-1。
(4)用x、y、z分别表示H2O、H2S、H2Se的沸点(℃),则x、y、z的大小关系______________________,其判断依据是______________________。
(12分)乙酸乙酯的实验室和工业制法常采用如下反应:
CH3COOH+C2H5OHCH3COOC2H5+H2O
请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有:________________、__________________等。
(2)若用如图(下右)所示装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为(填一点即可):____________________________________________________________________等。
(3)此反应以浓硫酸为催化剂,可能会造成(填一点即可)____________________等问题。
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯产品,下图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。
试剂a是 溶液,试剂b是 ,分离方法①是 ,分离方法②③都是 。E的结构简式为 ,在得到的A中加入无水碳酸钠粉末,振荡,目的是 。
C→D的离子方程式为 。
我国有许多燃煤电站,电站燃烧煤时产生了二氧化硫,为了减少二氧化硫的刺激,可在电站边建燃气脱硫工厂。工厂燃气脱硫工艺简图如图5-9所示。请根据以上材料,结合你所学的知识回答:

图5-9
(1)以上材料中,引起酸雨的人为因素是__________________。
(2)用化学方程式表示SO2形成酸雨的过程:__________________。
(3)酸雨不仅使土壤酸化,而且使土壤贫瘠,说明酸雨使土壤贫瘠的原因_________________。
(4)为减少电站在电能输送给远方时的能量损耗,采用何种输电方式比较合理?___________。
(5)脱硫工艺简图中,A是________,B是_______(填物质名称)。
(6)你认为应该如何控制酸雨污染物,防止酸雨危害?______________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com