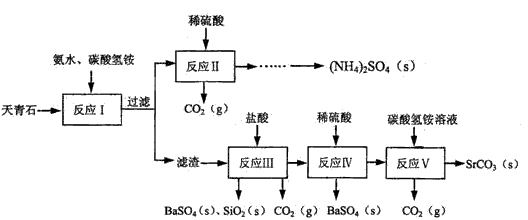
(2011?南京三模)碳酸锶大量用于生产彩色电视显像管的荧光屏玻璃.工业上常以天青石(主要成分为硫酸锶,含少量硫酸钡、二氧化硅等不溶性杂质)为原料制取碳酸锶.其工艺流程如下:

已知:K
sp(SrSO
4)=3.2×10
-7、K
sp(SrCO
3)=1.1×10
-10、K
sp(BaSO
4)=1.1×10
-10、K
sp(BaCO
3)=5.1×10
-9(1)反应I中需将天青石粉碎,其目的是
增加反应物的接触面积,提高反应速率,提高原科的利用率
增加反应物的接触面积,提高反应速率,提高原科的利用率
.
(2)反应I在65~80℃进行,碳酸氢铵的用量大于理论量,其原因可能是
反应中有部分碳酸氢铵会分解
反应中有部分碳酸氢铵会分解
.
(3)反应Ⅱ加硫酸的目的是
使碳酸铵、碳酸氢铵转化为硫酸铵
使碳酸铵、碳酸氢铵转化为硫酸铵
.
(4)反应Ⅲ中除了SrCO
3与盐酸反应外,发生的另一反应的离子方程式为
BaCO3+2H+=Ba2++CO2↑十H2O
BaCO3+2H+=Ba2++CO2↑十H2O
.
(5)反应V中生成SrCO
3的离子方程式为
Sr2++2HCO3-=SrCO3↓+CO2↑+H2O
Sr2++2HCO3-=SrCO3↓+CO2↑+H2O
.