
题目列表(包括答案和解析)
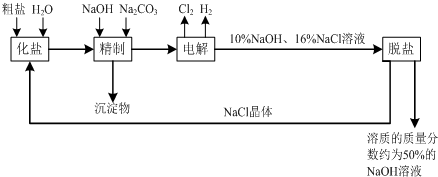
工业上用电解法制烧碱的主要原料是饱和食盐水,它是将粗盐溶于水制成的.由于粗盐水中含有泥沙、CaCl2、MgCl2、Fe2(SO4)3等杂质,不符合电解要求,因此必须经过精制.
将粗盐水过滤以后再用化学药品作进一步的净化.
(1)下列化学药品中可以选用的是(填写代号)________.
A.Ba(NO3)2 B.BaCl2 C.NaOH D.K2CO3 E.Na2CO3 F.盐酸 G.硫酸
(2)所选的化学药品要按一定的先后顺序向盐水中加入,请按这个顺序写出有关的化学反应方程式(化学药品都是加到稍过量的程度)________.
(3)在你设计的加入化学药品先后顺序里,在加入某种化学药品之前,还必须增加一种物理除杂方法.这种化学药品的名称是________,这种物理除杂方法的名称是________.要在实验室中实施这种方法,所用到的玻璃质实验仪器一般是(写仪器名称)________.
(4)经过分析,上述净化盐水的方案合理无误.又通过更加精确的实验方法对净化以后的盐水进行成分分析,发现其仍然含有影响饱和食盐水电解的CaCl2和MgCl2,必须进一步地减少其含量.对此,下列说法中正确的是(填写代号)________.
A.对盐水进行重新过滤除杂
B.再从上述的(1)中选择化学药品用化学方法除杂
C.查阅资料或访问专家,采用更加科学先进的方法进行除杂
工业上用电解法制烧碱的主要原料是饱和食盐水,它是将粗盐溶于水制成的.由于粗盐水中含有泥沙、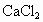 、
、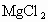 、
、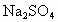 等杂质,不符合电解要求,因此必须经过精制.
等杂质,不符合电解要求,因此必须经过精制.
将粗盐水过滤以后再用化学药品作进一步的净化.
(1)下列化学药品中可以选用的是(填写代号)___________。
A. B.
B.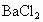 C.NaOH D.
C.NaOH D.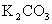 E.
E.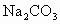 F.盐酸 G.硫酸
F.盐酸 G.硫酸
(2)所选的化学药品要按一定的先后顺序向粗盐水中加入,请按这个顺序写出有关化学反应的方程式(化学药品都是加到稍过量的程度)_________
_________。
(3)在你设计的加入化学药品先后顺序里,在加入某种化学药品之前,还必须增加一个物理除杂方法.这种化学药品的名称是______,这种物理除杂方法的名称是______。要在实验室中实施这种方法,所用到的玻璃质实验仪器一般是(写仪器名称)_______。
工业上用电解法制烧碱的主要原料是饱和食盐水,它是将粗盐溶于水制成的.由于粗盐水中含有泥沙、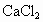 、
、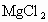 、
、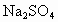 等杂质,不符合电解要求,因此必须经过精制.
等杂质,不符合电解要求,因此必须经过精制.
将粗盐水过滤以后再用化学药品作进一步的净化.
(1)下列化学药品中可以选用的是(填写代号)___________。
A.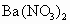 B.
B.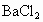 C.NaOH D.
C.NaOH D.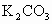 E.
E.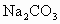 F.盐酸 G.硫酸
F.盐酸 G.硫酸
(2)所选的化学药品要按一定的先后顺序向粗盐水中加入,请按这个顺序写出有关化学反应的方程式(化学药品都是加到稍过量的程度)_________
_________。
(3)在你设计的加入化学药品先后顺序里,在加入某种化学药品之前,还必须增加一个物理除杂方法.这种化学药品的名称是______,这种物理除杂方法的名称是______。要在实验室中实施这种方法,所用到的玻璃质实验仪器一般是(写仪器名称)_______。


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com