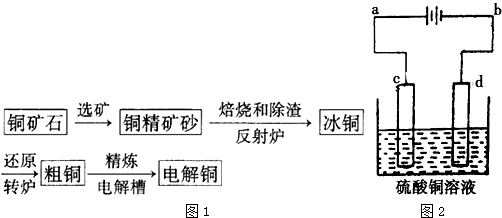
铜在自然界中多以硫化物存在,以黄铜矿(CuFeS
2)为原料冶炼精铜的工艺流程图如下:

(1)黄铜矿在反射炉中焙烧时,生成Cu
2S和FeS,请写出反应的化学方程式:
2CuFeS2+O2═Cu2S+2FeS+SO2
2CuFeS2+O2═Cu2S+2FeS+SO2
,生成的FeS继续在反射炉中进一步氧化:2FeS+3O
22FeO+2SO
2(2)焙烧后的矿砂与砂子混合,在反射炉中加热至1000℃熔融,其目的是:
①使Cu
2S和剩余的FeS熔融形成“冰铜”,转移到转炉中继续冶炼;
②
FeO与SiO2反应生成FeSiO3,成炉渣被除去
FeO与SiO2反应生成FeSiO3,成炉渣被除去
.
(3)大多数这样的冶炼厂都有一座附设工厂,该附设工厂的产品是
硫酸
硫酸
,其意义在于
节约资源,不污染环境
节约资源,不污染环境
.
(4)“冰铜”在转炉中熔炼,主要发生两个反应,首先是:2Cu
2S+3O
22Cu
2O+2SO
2,再由Cu
2O与Cu
2S反应制得单质铜.请写出该反应的化学方程式
2Cu2O+Cu2S═6Cu+SO2
2Cu2O+Cu2S═6Cu+SO2
.制得的铜块呈泡状(又称为泡铜),其原因是
由于冶炼出来的铜溶有的二氧化硫不断放出
由于冶炼出来的铜溶有的二氧化硫不断放出
.
(5)请简述粗铜精炼电解得到精铜的原理:
以硫酸铜-硫酸溶液为电解液.电解时,作阳极的粗铜中的铜以及比铜活泼的金属失去电子进入溶液,比铜不活泼的金属沉入电解槽形成“阳极泥”,溶液中的Cu2+得到电子沉积在阴极上
以硫酸铜-硫酸溶液为电解液.电解时,作阳极的粗铜中的铜以及比铜活泼的金属失去电子进入溶液,比铜不活泼的金属沉入电解槽形成“阳极泥”,溶液中的Cu2+得到电子沉积在阴极上
.