
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
| AЁЂЦППкИННќЕФШмвКНЯЯЁ | BЁЂЦПЕзИННќЕФШмвКНЯХЈ | CЁЂЦПЕзЛсгаЙЬЬхЮіГі | DЁЂЦПФкИїВПЗжШмвКЕФХЈЖШЖМЯрЭЌ |
 ЃЈ2013?БѕжнвЛФЃЃЉЃЈ1ЃЉФГбЇЯАаЁзщРћгУЯТЭМзАжУжЦШЁТШЦјВЂЬНОПЦфаджЪЃЎ
ЃЈ2013?БѕжнвЛФЃЃЉЃЈ1ЃЉФГбЇЯАаЁзщРћгУЯТЭМзАжУжЦШЁТШЦјВЂЬНОПЦфаджЪЃЎ
| ||
| ||
| ЪЕбщВНжш | дЄЦкЯжЯѓКЭНсТл | |
| Ђй | гУAЪдЙмШЁЩйСПГЮЧхЪЏЛвЫЎБИгУЃЌгУBЪдЙмШЁЩйСПбљЦЗЃЌдйЯђBЪдЙм МгШыЪЪСП1mol/LЕФбЮЫсЃЌШћЩЯДјЕМЙмЕФЕЅПзШћЃЌНЋЕМЙмЕФСэвЛЖЫВхШыAЪдЙмжа МгШыЪЪСП1mol/LЕФбЮЫсЃЌШћЩЯДјЕМЙмЕФЕЅПзШћЃЌНЋЕМЙмЕФСэвЛЖЫВхШыAЪдЙмжа |
ШєЮоЦјЬхЗХГіЧвГЮЧхЪЏЛвЫЎЮДМћЛызЧЃЌдђМйЩшвЛГЩСЂЃЛ ШєгаЦјХнУАГіЃЌЧвГЮЧхЪЏЛвЫЎБфЛызЧдђМйЩшвЛВНГЩСЂЃЌМйЩшЖўЁЂШ§ГЩСЂ ШєгаЦјХнУАГіЃЌЧвГЮЧхЪЏЛвЫЎБфЛызЧдђМйЩшвЛВНГЩСЂЃЌМйЩшЖўЁЂШ§ГЩСЂ |
| Ђк | гУНКЭЗЕЮЙмЯђЩЯЪіВНжшКѓЕФBЪдЙмжаЕЮШыМИЕЮЦЗКьЪдвКЃЌеёЕД гУНКЭЗЕЮЙмЯђЩЯЪіВНжшКѓЕФBЪдЙмжаЕЮШыМИЕЮЦЗКьЪдвКЃЌеёЕД |
ШєЦЗКьШмвКВЛЭЪЩЋЃЌдђМйЩшЖўГЩСЂЃЌШєЦЗКьШмвКЭЪЩЋЃЌдђМйЩшШ§ГЩСЂ ШєЦЗКьШмвКВЛЭЪЩЋЃЌдђМйЩшЖўГЩСЂЃЌШєЦЗКьШмвКЭЪЩЋЃЌдђМйЩшШ§ГЩСЂ |
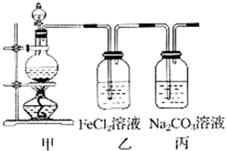
ЃЈ1ЃЉФГбЇЯАаЁзщРћгУЯТЭМзАжУжЦШЁТШЦјВЂЬНОПЦфаджЪЁЃ
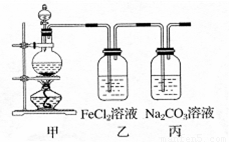
ЂйМззАжУжаЗДгІЕФЛЏбЇЗНГЬЪНЪЧ ЃЛ
ЂкжЄУїввзАжУжаFeCl2ШмвКгыCl2ЗЂЩњСЫЗДгІЕФЪЕбщЗНЗЈЪЧЃЈжЛзЂУїЪдМСЁЂЯжЯѓЃЉ ЃЛ
ЂлБћзАжУжаЭЈШыЩйСПCl2ЃЌПЩжЦЕУФГжжЩњЛюжаГЃгУЕФЦЏАзЁЂЯћЖОЕФЮяжЪЁЃвбжЊЬМЫсЕФЫсадЧПгкДЮТШЫсЃЌдђБћжаЗДгІЕФЛЏбЇЗНГЬЪНЪЧ ЁЃ
ЃЈ2ЃЉгавЛЦПГЄЦкЗХжУЕФЦЏАзЗлЃЌЧыРћгУвдЯТвЧЦїКЭЪдМСЃЌЭъГЩИУЦЏАзЗлГЩЗнЕФЬНОПЁЃ
ЪдЙмЁЂНКЭЗЕЮЙмЁЂДјЕМЙмЕФЕЅПзШћЁЂеєСѓЫЎЁЂ1molЁЄL-1бЮЫсЁЂЦЗКьШмвКЁЂаТжЦГЮЧхЪЏЛвЫЎЁЃ
ЁОЬсГіМйЩшЁПМйЩшвЛЃКИУЦЏАзЗлЮДБфжЪЃЌКЌCaCl2ЁЂCaЃЈClOЃЉ2ЃЛ
МйЩшЖўЃКИУЦЏАзЗлШЋВПБфжЪЃЌКЌ ЃЛ
МйЩшШ§ЃКИУЦЏАзЗлВПЗжБфжЪЃЌКЌCaCl2ЁЂCaЃЈClOЃЉ2ЁЂCaCO3 ЁЃ
ЁОНјааЪЕбщЁПдкД№ЬтПЈЩЯЭъГЩЯТБэЃЈВЛБиМьбщCa2+ЁЂCl-ЃЉЃК
|
ЪЕбщВНжш |
дЄЦкЯжЯѓКЭНсТл |
|
|
Ђй |
гУAЪдЙмШЁЩйСПГЮЧхЪЏЛвЫЎБИгУЃЌгУBЪдЙмШЁЩйСПбљЦЗЃЌдйЯђBЪдЙм
|
ШєЮоЦјЬхЗХГіЧвГЮЧхЪЏЛвЫЎЮДМћЛызЧЃЌдђМйЩшвЛГЩСЂЃЛ
|
|
Ђк |
|
|
| ЪЕбщВНжш | дЄЦкЯжЯѓКЭНсТл | |
| Ђй | гУAЪдЙмШЁЩйСПГЮЧхЪЏЛвЫЎБИгУЃЌгУBЪдЙмШЁЩйСПбљЦЗЃЌдйЯђBЪдЙм | ШєЮоЦјЬхЗХГіЧвГЮЧхЪЏЛвЫЎЮДМћЛызЧЃЌдђМйЩшвЛГЩСЂЃЛ |
| Ђк | ||

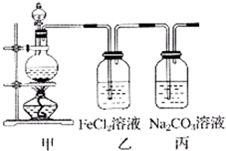 ЃЈ1ЃЉФГбЇЯАаЁзщРћгУЯТЭМзАжУжЦШЁТШЦјВЂЬНОПЦфаджЪЃЎ
ЃЈ1ЃЉФГбЇЯАаЁзщРћгУЯТЭМзАжУжЦШЁТШЦјВЂЬНОПЦфаджЪЃЎ| ЪЕбщВНжш | дЄЦкЯжЯѓКЭНсТл | |
| Ђй | гУAЪдЙмШЁЩйСПГЮЧхЪЏЛвЫЎБИгУЃЌгУBЪдЙмШЁЩйСПбљЦЗЃЌдйЯђBЪдЙм______ | ШєЮоЦјЬхЗХГіЧвГЮЧхЪЏЛвЫЎЮДМћЛызЧЃЌдђМйЩшвЛГЩСЂЃЛ______ |
| Ђк | ______ | ______ |
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com