
题目列表(包括答案和解析)
(13分)下表为周期表的一部分,表中所列的字母分别代表一种化学元素。
|
a |
|
|
|
|
|||||||||||||
|
|
|
|
|
b |
c |
d |
|
|
|||||||||
|
|
|
|
|
|
e |
f |
|
|
|||||||||
|
|
|
|
|
|
g |
|
h |
|
|
|
|
|
|
|
|
|
|
用化学用语回答下列问题:
(1)写出元素g的基态原子核外电子排布式___________________________,
h2+中未成对电子数为 。
(2)在b2a2分子中,元素b为 杂化,该分子是 分子(填“极性”或“非极性”),该分子中σ键和π键的数目比为 。
(3) bd2与bf2比较,沸点较高的是_______(填分子式),原因是 。
(4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙正确是 。
A.h位于元素周期表中第四周期第VIII族,属于d区元素
B.e的基态原子中,3p能级为半充满,属于p区元素
C.最外层电子排布式为4s2,一定属于IIA族
D.最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族
(5)科学研究表明,元素b与元素c可以形成一种超硬、耐磨、耐高温的新型无机非金属材料,其化学式为 ,其熔点比金刚石 (填“高”或“低”)。
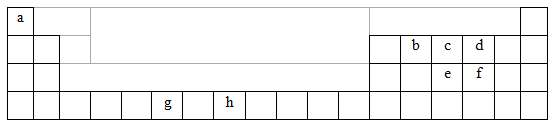
下表为周期表的一部分,表中所列的字母分别代表一种化学元素。
| a | |||||||||||||||||
| b | c | d | |||||||||||||||
| e | f | ||||||||||||||||
| g | h | ||||||||||||||||
用化学用语回答下列问题:
(1)写出元素g的基态原子核外电子排布式____________,h2+中未成对电子数为 ![]() 。
。
(2)在b2a2分子中,元素b为 杂化,![]() 该分子是 分子(填“极性”或“非极性”),该分子中σ键和π键的数目比为 。
该分子是 分子(填“极性”或“非极性”),该分子中σ键和π键的数目比为 。
(3)bd2与bf2比较,沸点较高的是_______(填分子式),原因是 。
(4)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙正确是 。
A、h位于元素周期表中第四周期第VIII族,属于d区元素
B、e的基态原子中,3p能级为半充满,属于p区元素
C、最外层电子排布式为4s2,一定属于IIA族
D、最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族
(5)科学研究表明,元素![]() b与元素c可以形成一种超硬、耐磨、耐高温的新型无机非金属材料,其化学式为 ,其熔点比金刚石 (填“高”或“低”)。
b与元素c可以形成一种超硬、耐磨、耐高温的新型无机非金属材料,其化学式为 ,其熔点比金刚石 (填“高”或“低”)。
国际无机化学命名委员会在1989年作出决定,把长式周期表原先的主、副族及族号取消,从左到右改为第1~18列,如氢和碱金属为第1列,稀有气体元素族为第18列。按这个规定,下列说法不正确的是
A.第15列元素(用R表示)的最高价氧化物通式为R2O5
B.第3列元素种类最多、第14列元素的化合物种类最多
C.第VIII族包括8、9、10三列
D.最外层有2个电子的元素都在第2列,第2列元素中肯定没有非金属元素
| 元素 | 相关信息 |
| X | X的基态原子L层电子数是K层电子数的2倍 |
| Y | Y的基态原子最外层电子排布式为:nsnnpn+2 |
| Z | Z存在质量数为23,中子数为12的核素 |
| W | W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com