
ĖâÄŋÁÐąí(°üĀĻīð°ļšÍ―âÎö)
ĢĻ11·ÖĢĐļßĖúËážØĢĻK2FeO4ĢĐĘĮŌŧÖÖžŊŅõŧŊĄĒÎüļ―ĄĒÐõÄýÓÚŌŧĖåĩÄÐÂÐÍķāđĶÄÜËŪīĶĀížÁĄĢÆäÉúēúđĪŌÕČįÏÂĢš
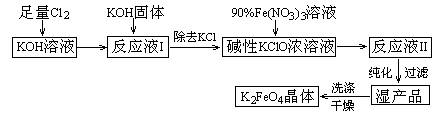
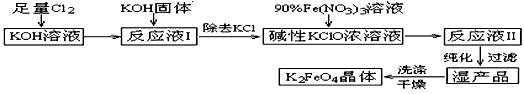
ŌŅÖŠĢšĒŲ 2KOH + Cl2 Ąú KCl + KClO + H2OĢĻĖõžþĢšÎÂķČ―ÏĩÍĢĐ
ĒÚ 6KOH + 3Cl2 Ąú 5KCl + KClO3 + 3H2OĢĻĖõžþĢšÎÂķČ―ÏļßĢĐ
ĒÛ 2Fe(NO3)3 + 2KClO + 10KOH Ąú 2K2FeO4 + 6KNO3 + 3KCl + 5H2O
ŧØīðÏÂÁÐÎĘĖâĢš
ĒÅļÃÉúēúđĪŌÕÓĶÔÚ ĢĻĖÎÂķČ―ÏļߥąŧōĄ°ÎÂķČ―ÏĩÍĄąĢĐĩÄĮéŋöÏÂ―øÐÐĢŧ
ĒÆÐīģöđĪŌĩÉÏÖÆČĄCl2ĩÄŧŊŅ§·―ģĖĘ― Ģŧ
ĒĮK2FeO4ūßÓÐĮŋŅõŧŊÐÔĩÄÔŌō Ģŧ
ĒČÅäÖÆKOHČÜŌšĘąĢŽĘĮÔÚÃŋ100 mLËŪÖÐČÜ―â61.6 g KOHđĖĖåĢĻļÃČÜŌšĩÄÃÜķČΊ1.47 g/mLĢĐĢŽËüĩÄÎïÖĘĩÄÁŋÅĻķČΊ Ģŧ
ĒÉÔÚĄ°·īÓĶŌšIĄąÖОÓKOHđĖĖåĩÄÄŋĩÄĘĮ Ģš
AĢŪÓ륰·īÓĶŌšIĄąÖÐđýÁŋĩÄCl2žĖÐø·īÓĶĢŽÉúģÉļüķāĩÄKClO
BĢŪKOHđĖĖåČÜ―âĘąŧá·Åģö―ÏķāĩÄČČÁŋĢŽÓÐĀûÓÚĖáļß·īÓĶËŲÂĘ
CĢŪΊÏÂŌŧē―·īÓĶĖáđĐ·īÓĶÎï
DĢŪĘđļąēúÎïKClO3ŨŠŧŊΊ KClO
(ČýŅĄŌŧ----ŧŊŅ§ÓëžžĘõ)
ļßĖúËážØĢĻK2FeO4ĢĐĘĮŌŧÖÖžŊŅõŧŊĄĒÎüļ―ĄĒÐõÄýÓÚŌŧĖåĩÄÐÂÐÍķāđĶÄÜËŪīĶĀížÁĄĢÆäÉúēúđĪŌÕČįÏÂĢš

ÔÄķÁÏÂÁÐēÄÁÏšóĢŽŧØīðÏāÓĶÎĘĖâĢŪ
ŌŧļöĖåÖØ50 KgĩÄ―ĄŋĩČËīóÔžšŽĖú2 gĢŽÕâ2 gĖúÔÚČËĖåÖÐēŧĘĮŌÔĩĨÖĘ―ðĘôÐÎĘ―īæÔÚĢŽķøĘĮŌÔFe2+šÍFe3+ĩÄÐÎĘ―īæÔÚĢŪķþžÛĖúĀëŨÓŌŨąŧÎüĘÕĢŽļøÆķŅŠÕßēđģäĖúĘąĢŽÓĶļøÓ蚎ķþžÛĖúĀëŨÓĩÄķþžÛĖúŅÎĢŽČįÁōËáŅĮĖú(FeSO4)ĢŪ·þÓÃÎŽÉúËØCĢŽŋÉĘđĘģÎïÖÐĩÄČýžÛĖúĀëŨÓŧđÔģÉķþžÛĖúĀëŨÓĢŽÓÐĀûÓÚĖúĩÄÎüĘÕĢŪ
(1)ČËĖåÖÐūģĢ―øÐÐFe2ĢŦ![]() Fe3ĢŦĩÄÏāŧĨŨŠŧŊĢŽÔÚAđýģĖÖÐĢŽFe2+Ũö________žÁĢŽÔÚBđýģĖÖÐĢŽFe3+Ũö________žÁĢŪ
Fe3ĢŦĩÄÏāŧĨŨŠŧŊĢŽÔÚAđýģĖÖÐĢŽFe2+Ũö________žÁĢŽÔÚBđýģĖÖÐĢŽFe3+Ũö________žÁĢŪ
(2)Ą°·þÓÃÎŽÉúËØCĢŽŋÉĘđĘģÎïÖÐČýžÛĖúĀëŨÓŧđÔģÉķþžÛĖúĀëŨÓĢŪĄąÕâūäŧ°ÖļģöĢŽÎŽÉúËØCÔÚÕâŌŧ·īÓĶÖÐŨö________žÁĢŽūßÓÐ________ÐÔĢŪ
(3)ŌŅÖŠĢšŅõŧŊÐÔCl2ĢūBr2ĢūFe3+ĢŽŧđÔÐÔFe2+ĢūBrĢĢūClĢĢŽÔōÏō0.2 mol/LĄĄ1 LĄĄFeBr2ČÜŌšÖÐÍĻČëąęŨžŨīŋöÏÂÂČÆø2.24 LĢŽąŧŅõŧŊĩÄÁĢŨÓĘĮ________ĢŽīË·īÓĶĩÄĀëŨÓ·―ģĖĘ―Ģš________ĢŪ

| žÓČČ |
| žÓČČ |
| žÓČČ |
| ||
| ||
đúžĘŅ§ÐĢÓÅŅĄ - Á·Ï°ēáÁÐąí - ĘÔĖâÁÐąí
šþąąĘĄŧĨÁŠÍøÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻÆ―ĖĻ | ÍøÉÏÓКĶÐÅÏĒūŲąĻŨĻĮø | ĩįÐÅÕĐÆūŲąĻŨĻĮø | ÉæĀúĘ·ÐéÎÞÖũŌåÓКĶÐÅÏĒūŲąĻŨĻĮø | ÉæÆóĮÖČĻūŲąĻŨĻĮø
ÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻĩįŧ°Ģš027-86699610 ūŲąĻÓĘÏäĢš58377363@163.com