
题目列表(包括答案和解析)
下列有关实验的结论正确的是
选项 实验操作及现象 实验结论
A 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 溶液中一定含有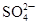
B 向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色气体 溶液中一定含有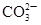
C 用酸度计测定SO2和CO2饱和溶液的pH,前者pH小 H2SO3酸性强于H2CO3
D 用玻璃棒蘸取浓氨水点到红色石蕊试纸上,试纸变蓝色 浓氨水呈碱性
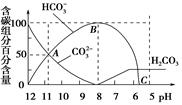
常温下在20 mL 0.1 mol/L Na2CO3溶液中逐渐滴加入0.1 mol/L HCl溶液40 mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示,下列说法不正确的是
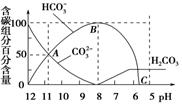
A.0.1 mol/L Na2CO3溶液中c(OH-)-c(H+)=2c(H2CO3)+c(HCO3-)
B.在A点c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
C.常温下CO2饱和溶液的pH约为5.6
D.0.05 mol/L NaHCO3溶液的pH=8
A.2 B.3 C.5.6 D.8
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com