
题目列表(包括答案和解析)
|
以Al、稀H2SO4和NaOH为原料制取Al(OH)3,甲、乙、丙3个学生分别用3种不同的途径制备: 甲:Al 乙:Al
若要制得等量的Al(OH)3,则 | |
| [ ] | |
A. |
乙消耗原料最少 |
B. |
三者消耗原料相同 |
C. |
丙消耗的原料最少 |
D. |
甲、乙消耗原料相同 |
用稀H2SO4、NaOH溶液和废铝为原料制取Al(OH)3,甲、乙、丙三位同学的制备途径如下,请对此回答问题:
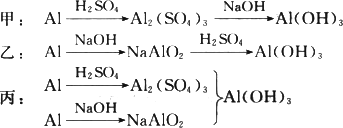
(1)在三个方案中,其中有一个的化学变化里涉及到两种盐在溶液中发生反应,写出该化学反应的离子方程式:________.
(2)从获得同样多的产品而原料用量最少的角度来看,三个方案中最理想的是________.在你认为不够理想的方案中,除去原料消耗量的因素以外,还有方案不理想的理由是(任选一个方案谈一个主要理由)________.
(3)在你认为理想的方案中,为了达到使一定质量的废铝充分利用的目的,在方案实施之前,还要做的定量实验是________.
①2Al+3H2SO4====Al2(SO4)3+3H2↑
Al2(SO4)3+6NaOH====2Al(OH)3↓+3Na2SO4
②2Al+2NaOH+2H2O====2NaAlO2+3H2↑
2NaAlO2+H2SO4+2H2O====2Al(OH)3↓+Na2SO4
(1)请将每制取2 mol Al(OH)3所耗费的酸、碱用量记录于下表中,然后说明哪一种方法比较节约试剂。
途 径 | 生成2 mol Al(OH)3所消耗酸碱的物质的量 | |
| n(H2SO4)/mol | n(NaOH)/mol |
①Al→Al3+→Al(OH)2 ②Al→ |
|
|
(2)原料相同,请设计一种更节约试剂,且操作更为简单的方法,(提示:从反应终点是否易于控制角度考虑)。用化学方程式表示并予以说明。
(20分)某化学课外活动小组以铝屑、稀H2SO4、NaOH溶液为主要原料欲制备Al(OH)3沉淀,设计了如下三种方案,见下表。阅读下表并回答下列问题:
| 途径 | 生成1 mol Al(OH)3消耗H+或OH-的物质的量/mol | |
| 消耗H+ | 消耗OH- | |
| 1.Al→Al3+→Al(OH)3 | | |
2.Al→AlO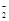 →Al(OH)3 →Al(OH)3 | | |
3.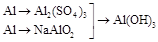 | | |
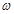 (g)NaOH固体。他在托盘天平的右盘上放入(
(g)NaOH固体。他在托盘天平的右盘上放入(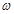 + y)(g)砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,如图所示,下面他的操作应该是_________ 使 。
+ y)(g)砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,如图所示,下面他的操作应该是_________ 使 。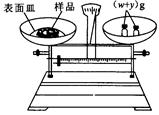
 (g)NaOH刚好可配制0.5mol·L-1NaOH溶液500mL。在下列配制溶液过程示意图中有错误的是(填操作序号)______________。
(g)NaOH刚好可配制0.5mol·L-1NaOH溶液500mL。在下列配制溶液过程示意图中有错误的是(填操作序号)______________。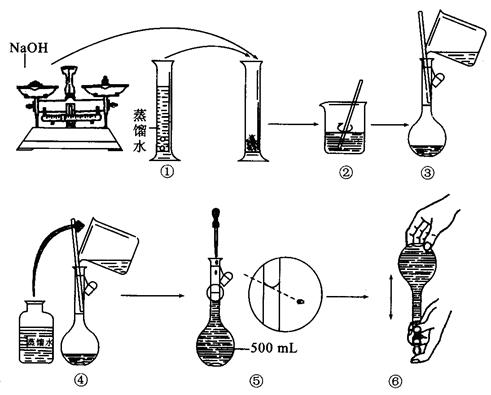
 NaOH溶液,再加入足量铝屑。给溶液稍加热。其作用是:__________________________用蒸馏水把铝屑冲洗干净。称量铝屑的质量为m1(g)。
NaOH溶液,再加入足量铝屑。给溶液稍加热。其作用是:__________________________用蒸馏水把铝屑冲洗干净。称量铝屑的质量为m1(g)。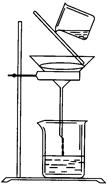
(20分)某化学课外活动小组以铝屑、稀H2SO4、NaOH溶液为主要原料欲制备Al(OH)3沉淀,设计了如下三种方案,见下表。阅读下表并回答下列问题:
|
途径 |
生成1 mol Al(OH)3消耗H+或OH-的物质的量/mol |
|
|
消耗H+ |
消耗OH- |
|
|
1.Al→Al3+→Al(OH)3 |
|
|
|
2.Al→AlO |
|
|
|
3. |
|
|
(1)填写上表中空格并从节约原料的角度来分析,你认为应选择方案_________最为合理。
(2)本实验要用到NaOH溶液。某学生用已知质量y(g)的表面皿,准确称取 (g)NaOH固体。他在托盘天平的右盘上放入(
(g)NaOH固体。他在托盘天平的右盘上放入( + y)(g)砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,如图所示,下面他的操作应该是_________ 使
。
+ y)(g)砝码,在左盘的表面皿中加入NaOH固体,这时指针偏向右边,如图所示,下面他的操作应该是_________ 使
。

(3)若称取的 (g)NaOH刚好可配制0.5mol·L-1NaOH溶液500mL。在下列配制溶液过程示意图中有错误的是(填操作序号)______________。
(g)NaOH刚好可配制0.5mol·L-1NaOH溶液500mL。在下列配制溶液过程示意图中有错误的是(填操作序号)______________。

(4)阅读下列制备Al(OH)3实验步骤,填写空白:
①在烧杯A中加入50mL0.5mol·L NaOH溶液,再加入足量铝屑。给溶液稍加热。其作用是:__________________________用蒸馏水把铝屑冲洗干净。称量铝屑的质量为m1(g)。
NaOH溶液,再加入足量铝屑。给溶液稍加热。其作用是:__________________________用蒸馏水把铝屑冲洗干净。称量铝屑的质量为m1(g)。
②在盛有适量稀H2SO4的烧杯B中应放入___________(g)(用含m1的式子表示)质量的铝屑,充分搅拌使铝屑反应完全。
③在盛有适量浓NaOH溶液的烧杯C中放入____________(g)(用含m1的式子表示)质量的铝屑充分搅拌使铝屑反应完全。
④将烧杯B和烧杯C中的溶液混和观察到的现象是:_______________________________,反应的离子方程式是:___________________________
(5)过滤时某学生操作如图,请用文字说明图中错误的是:
_____________________ 。

(6)把沉淀转移到烧杯中,用蒸馏水洗涤三次再过滤,再洗涤、
干燥得Al(OH)3固体质量为m2(g)计算本实验Al(OH)3的产率是_________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com