
题目列表(包括答案和解析)
(8分)请根据反应 :Fe + Cu2+ = Fe 2++Cu 设计原电池:
(1) (2分)画出实验的简易装置图:(用铅笔画图)
(2)(6分)写出电极反应式,正极: ,负极: 。当反应进行到一段时间后取出电极材料,测得某一电极增重了6.4g,则反应共转移了的电子数是 。
(10分)某学生设计了一个制取氢氧化亚铁的最佳实验方案,实验装置见图,请分析实验过程:

⑴在B试管中加入NaOH溶液后加热煮沸1—2分
钟立即加入2mL液体石蜡,该操作目的是_______________ ________。
⑵在具支试管A中加入稀H2SO4溶液和略微过量的铁粉,分析为什么铁粉过量_________________________。
⑶连接好导管,同时打开活塞,当铁粉与稀硫酸反应平稳时,关闭活塞,这时A试管中的现象为____________________,原因是_______ 。B试管中现象为__ 。
(8分)请根据反应 :Fe + Cu2+ = Fe 2++ Cu 设计原电池:
(1) (2分)画出实验的简易装置图:(用铅笔画图)
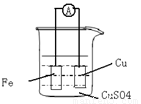
(2)(6分)写出电极反应式,正极: ,负极: 。当反应进行到一段时间后取出电极材料,测得某一电极增重了6.4g,则反应共转移了的电子数是 。
(8分)欲配制100mL 0.2mol/L的NaOH溶液,回答下列问题:
(1) (2分)根据计算,所需的NaOH的质量为 ,NaOH固体应放在 中称量。(2) (3分)以下是实验操作步 骤,请排出正确的操作顺序:
骤,请排出正确的操作顺序:
①称取所需质量的NaOH
②将溶液转移到容量瓶内
③用蒸馏水洗涤烧杯2~3次,将洗涤液全部移入容量瓶中,摇匀
④改用胶头滴管,小心滴入蒸馏水至刻度
⑤仔细地把蒸馏水注入容量瓶中,直到液面接近刻度线1cm~2cm处
⑥塞上瓶塞。反复摇匀
⑦将称取的NaOH置于烧杯内,加适量蒸馏水,搅拌溶解后冷却
正确的操作顺序是:
(3) (3分)下列操作会使所配溶液浓度偏低的是 (填选项代号)
| A.NaOH放在纸上称量,且出现潮解现象 |
| B.配制前容量瓶内已有少量蒸馏水 |
| C.定容时仰视 |
| D.NaOH溶液未经冷却就转移到容量瓶中去 |
(8分)请根据反应:Fe + Cu2+ = Fe 2++ Cu 设计原电池:
(1) (2分)画出实验的简易装置图:(用铅笔画图)
(2)(6分)写出电极反应式,正极: ,负极: 。当反应进行到一段时间后取出电极材料,测得某一电极增重了6.4g,则反应共转移了的电子数是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com