
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
A°¢B°¢C°¢DÀƒ÷÷∂Ã÷Ð∆⁄‘™Àÿµƒ‘≠◊”∞Îæ∂“¿¥Œºı–°£¨DƒÐ∑÷±”ÎA°¢B°¢C–Œ≥…µÁ◊”◊Ð ˝œýµ»µƒ∑÷◊”X°¢Y°¢Z£ÆC‘≠◊”µƒ◊ÓÕ‚≤„µÁ◊”≈≈≤ºŒ™nsnnp2n£ÆEµƒ‘≠◊”–Ú ˝Œ™29£Æ
(1)A°¢B°¢Cµƒµ⁄“ªµÁ¿ÎƒÐ”…–°µΩ¥ÛµƒÀ≥–ÚŒ™________(”√‘™Àÿ∑˚∫≈±Ì æ)£Æ
(2)X «∫¨”–________º¸(ÃÓ°∞∑«º´–‘°±ªÚ°∞º´–‘°±£¨œ¬Õ¨)µƒ________∑÷◊”£Æ
(3)Aµƒ“ª÷÷«‚ªØŒÔœý∂‘∑÷◊”÷ ¡øŒ™26£¨∆‰∑÷◊”÷–µƒ¶“º¸”ζ–º¸µƒº¸ ˝÷Ʊ»Œ™________£Æ
(4)Y∑÷◊”µƒø’º‰ππ–ÕŒ™________£¨∆‰÷––ƒ‘≠◊”≤…»°________‘”ªØ£Æ
(5)“ª÷÷”…B°¢C◊È≥…µƒªØ∫œŒÔ”ÎAC2ª•Œ™µ»µÁ◊”ã¨∆‰ªØ—ß ΩŒ™________£Æ
(6)Y «“ª÷÷“◊“∫ªØµƒ∆¯Ã£¨«ÎºÚ ˆ∆‰“◊“∫ªØµƒ‘≠“Ú________________£Æ
(7)–¥≥ˆE2+µƒµÁ◊”≈≈≤º Ω________£¨≤¢–¥≥ˆE2+‘⁄Z÷–Õ®»Î◊„¡øYµ√µΩ…Ó¿∂…´»Ð“∫µƒ¿Î◊”∑Ω≥à Ω________£Æ
‘™Àÿ | ∑˚∫≈ | √˚≥∆ | Àƒ÷÷‘™Àÿµ•÷ º‰µƒ∑¥”¶ |
A |
|
|
|
B |
|
| |
C |
|
| |
D |
|
|
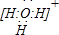
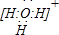




£®14∑÷£©Q°¢R°¢X°¢Y°¢ZŒÂ÷÷‘™Àÿµƒ‘≠◊”–Ú ˝“¿¥Œµð‘ˆ°£“—÷™£∫
¢ŸZµƒ‘≠◊”–Ú ˝Œ™29£¨∆‰”ýµƒæ˘Œ™∂Ã÷Ð∆⁄÷˜◊‘™Àÿ£ª
¢⁄Y‘≠◊”º€µÁ◊”£®Õ‚ŒßµÁ◊”£©≈≈≤ºmsnmpn
¢€R‘≠◊”∫ÀÕ‚L≤„µÁ◊” ˝Œ™∆Ê ˝£ª
¢ÐQ°¢X‘≠◊”pπϵ¿µƒµÁ◊” ˝∑÷±Œ™2∫Õ4°£
«Îªÿ¥œ¬¡–Œ £∫
£®1£©Z2+ µƒ∫ÀÕ‚µÁ◊”≈≈≤º Ω « °£
£®2£©‘⁄[Z(NH3)4]2+¿Î◊”÷–£¨Z2+µƒø’º‰πϵ¿ ÐNH3∑÷◊”Ã·π©µƒ –Œ≥…≈‰Œªº¸°£
£®3£©Q”ÎY–Œ≥…µƒ◊ÓºÚµ•∆¯Ã¨«‚ªØŒÔ∑÷±Œ™º◊°¢““£¨œ¬¡–≈–∂œ’˝»∑µƒ « °£
a.Œ»∂®–‘£∫º◊>““£¨∑–µ„£∫º◊>““ b.Œ»∂®–‘£∫º◊>““£¨∑–µ„£∫º◊>““
c.Œ»∂®–‘£∫º◊<““£¨∑–µ„£∫º◊<““ d.Œ»∂®–‘£∫º◊<““£¨∑–µ„£∫º◊>““
(4) Q°¢R°¢X°¢YÀƒ÷÷‘™Àÿµƒµ⁄“ªµÁ¿ÎƒÐ ˝÷µ”…–°µΩ¥ÛµƒÀ≥–ÚŒ™ £®”√‘™Àÿ∑˚∫≈◊˜¥£©
£®5£©Rµƒ«‚ªØŒÔµƒ»€∑–µ„±»Õ¨÷˜◊Â∆‰À¸‘™Àÿ«‚ªØŒÔµƒ»€∑–µ„∏þ£¨‘≠“Ú «R«‚ªØŒÔ________
________________________________________________________________________°£
£®6£©Qµƒ“ª÷÷«‚ªØŒÔœý∂‘∑÷◊”÷ ¡øŒ™26£¨∆‰÷–∑÷◊”÷–µƒ¶“º¸”ζ–º¸µƒº¸ ˝÷Ʊ»Œ™ °£
£®7£©ŒÂ÷÷‘™Àÿ÷–£¨µÁ∏∫–‘◊Ó¥Û”Î◊Ó–°µƒ¡Ω÷÷∑«Ω Ù‘™Àÿ–Œ≥…µƒæßàٔ⁄ °£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com