
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
(8·Ö)
ỈÑÖª2H2(g)+O2(g)=2H2O(g) ¡÷H=-483£®6 kJ£¯mol
2H2(g)+O2(g)=2H2O(l) ¡÷H=-571£®6 kJ£¯mol
(1)ÇâÆøµÄȼÉƠÈÈ¡÷H= kJ£¯mol
(2)ȼÉƠ2gH2Éú³ÉË®ƠôÆø£¬·Å³öµÄÈÈÁ¿Îª kJ¡£
¢̣°ÑĂº×÷ΪȼÁÏ¿Éͨ¹ưÏÂÁĐÁ½ÖÖ;¾¶»ñµĂÈÈÁ¿£º
;¾¶1£ºÖ±½ÓȼÉƠ
C(s)+O2(g)=CO2(g) ¡÷H=E1 ¢Ù
;¾¶2£ºÏÈÖƳÉË®ĂºÆø£¬ÔÙȼÉƠË®ĂºÆø
C(s)+H2O(g)=CO(g)+H2(g) ¡÷H=E2 ¢Ú
H2(g)+1£¯2 O2(g)=H2O(g) ¡÷H=E3 ¢Û
CO(g)+1£¯2 O2(g)=CO2(g) ¡÷H=E4 ¢Ü
Çë»Ø´đ£º
(1)ÉÏÊöËĸöÈÈ»¯Ñ§·½³̀ʽÖĐÄĸö·´Ó¦¡÷H >0? (̀îĐ̣ºÅ)
(2)µÈÖÊÁ¿µÄĂº·Ö±đͨ¹ửÔÉÏÁ½̀ơ²»Í¬µÄ;¾¶²úÉúµÄ¿ÉÀûÓõÄ×ÜÄÜÁ¿¹ØϵƠưÈ·µÄÊÇ
(̀îÑ¡Ïî×Öĸ)¡£
A£®Í¾¾¶1±È;¾¶2¶à B£®Í¾¾¶1±È;¾¶2ÉÙ C£®Í¾¾¶1Óë;¾¶2ÔÚÀíÂÛÉÏÏàͬ
(3)¸ù¾ƯÄÜÁ¿ÊØºă¶¨ÂÉ£¬E1¡¢E2¡¢E3¡¢E4Ö®¼äµÄ¹ØϵΪ £®
£¨Ă¿¿Ơ2·Ö£¬¹²8·Ö£©̉ÑÖªËÄÖÖÇ¿µç½âÖÊÈÜ̉º£¬·Ö±đº¬ÓĐÏÂÁĐ̉ơ¡¢ÑôÀë×ÓÖеĸ÷̉»ÖÖ![]() £¬²¢Ç̉»¥²»Öظ´£ºNH
£¬²¢Ç̉»¥²»Öظ´£ºNH![]() ¡¢Ba2£«¡¢Na£«¡¢H£«¡¢SO
¡¢Ba2£«¡¢Na£«¡¢H£«¡¢SO![]() ¡¢NO
¡¢NO![]() ¡¢OH£¡¢CO
¡¢OH£¡¢CO![]() ¡£½«ƠâËÄÖÖÈÜ̉º·Ö±đ±ê¼ÇΪA¡¢B¡¢C¡¢D£¬½øĐĐÈçÏÂʵÑ飺
¡£½«ƠâËÄÖÖÈÜ̉º·Ö±đ±ê¼ÇΪA¡¢B¡¢C¡¢D£¬½øĐĐÈçÏÂʵÑ飺
¢ÙÔÚA»̣DÖеÎÈëC£¬¾ùÓĐ³ÁµíÉú³É
¢ÚDºÍB·´Ó¦Éú³ÉµÄÆø̀åÄܱ»AÎüÊƠ
¢ÛAºÍD·´Ó¦Éú³ÉµÄÆø̀åÄܱ»BÎüÊƠ
ÊԻشđÏÂÁĐÎỀ⣺
£¨1£©DµÄ»¯Ñ§Ê½Êǣߣߣߣߣߣߣ¬ÅжÏÀíÓÉÊǣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߡ£
£¨2£©Đ´³öBÎïÖʵĻ¯Ñ§Ê½£ß£ß£ß£ß£ß¡£
£¨3£©Đ´³öDºÍB·´Ó¦µÄÀë×Ó·½³̀ʽ£ß£ß£ß£ß£ß£ß£ß£ß£ß£ß£ß£ß£ß£ß£ß£ß£ß£ß£ß¡£
£¨ 8·Ö£©̉ÑÖª°±Ë®µÄµçÀë¶ÈÓë´×ËáµÄµçÀë¶ÈÔÚͬÎÂͬŨ¶ÈÏÂÏàµÈ£¬ÈÜÓĐ̉»¶¨Á¿°±µÄÂÈ»¯ï§ÈÜ̉º³Ê¼îĐÔ¡£ÏÖỊ̈ÉÙÁ¿µÄMg(OH)2Đü×Ç̉ºÖĐ£¬¼ÓÈëÊÊÁ¿µÄ±¥ºÍÂÈ»¯ï§ÈÜ̉º£¬¹̀̀åÍêÈ«Èܽ⡣
¼×ͬѧµÄ½âÊÍÊÇ£ºMg(OH)2£¨¹̀£©Mg2£«£¨aq£©+2OH¡ª£¨aq£©¡¡¡¡¢Ù
NH4£«+H2ONH3¡¤H2O +H£«¡¡¡¡¢Ú H£«+OH¨D
H2O¡¡¡¡¢Û
ÓÉÓÚNH4£«Ë®½âÏÔËáĐÔ£¬H£«ÓëOH¨D·´Ó¦Éú³ÉË®£¬µ¼Ö·´Ó¦¢ÙƽºâÓ̉̉Æ£¬³ÁµíÈܽ⣻
̉̉ͬѧµÄ½âÊÍÊÇ£ºMg(OH)2£¨¹̀£©Mg2£«£¨aq£©+2OH¡ª£¨aq£©¡¡¢Ù NH4£«+OH¨D
NH3¡¤H2O¡¡¢Ú
ÓÉÓÚNH4ClµçÀë³öµÄNH4£«ÓëMg(OH)2µçÀë³öµÄOH¨D½áºÏ£¬Éú³ÉÁËÈơµÄµç½âÖÊNH3¡¤H2O£¬µ¼Ö·´Ó¦¢ÙµÄƽºâÓ̉̉Æ£¬Mg(OH)2³ÁµíÈܽ⡣
£¨1£©±ûͬѧ²»Äܿ϶¨ÄÄλͬѧµÄ½âÊͺÏÀí£¬ÓÚÊÇÑ¡ÓĂÏÂÁеÄ̉»ÖÖÊÔ¼Á£¬À´Ö¤Ă÷¼×¡¢̉̉Á½Î»Í¬Ñ§µÄ½âÊÍÖ»ÓĐ̉»ÖÖƠưÈ·£¬ËûÑ¡ÓõÄÊÔ¼ÁÊÇ £῭îĐ´±àºÅ£©¡£
A.NH4NO3 B.CH3COONH4 C.Na2CO3 D.NH3¡¤H2O
£¨2£©ÇëÄă˵Ă÷±ûͬѧ×÷³ö¸ĂÑ¡ÔñµÄÀíÓÉ ¡£
£¨3£©±ûͬѧ½«ËùÑ¡ÊÔ¼ÁµÎÈëMg(OH)2µÄ×Ç̉ºÖĐ£¬Mg(OH)2Èܽ⣻ÓÉ´ËÍÆÖª£¬¼×ºÍ̉̉ÄÄλͬѧµÄ½âÊ͸üºÏÀí £῭î¡°¼×¡±»̣¡°̉̉¡±£©£»Íê³ÉNH4Cl±¥ºÍÈÜ̉ºÊ¹Mg(OH)2Đü×Ç̉ºÈܽâµÄÀë×Ó·½³̀ʽ ¡£
£¨±¾̀â¹²8·Ö£©
̉ÑÖª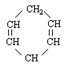 ¿É¼̣Đ´Îª
¿É¼̣Đ´Îª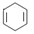 ¡£ÏÖÓĐij»¯ºÏÎïWµÄ·Ö×ӽṹ¿É±íʾΪ
¡£ÏÖÓĐij»¯ºÏÎïWµÄ·Ö×ӽṹ¿É±íʾΪ ¡£¸ù¾Ừẩâ»Ø´đ£º
¡£¸ù¾Ừẩâ»Ø´đ£º
1£®WÊôÓÚ
A£®·¼Ïằ₫ B£®»·̀₫ C£®²»±¥ºÍ̀₫ D£®È²̀₫
2£®WµÄ·Ö×ÓʽΪ £¬ËüµÄ̉»ÂÈ´úÎïÓĐ ÖÖ¡£
3£®ÓĐ¹ØWµÄ˵·¨´íÎóµÄÊÇ
A£®ÄÜ·¢Éú»¹Ô·´Ó¦ B£®ÄÜ·¢ÉúÑơ»¯·´Ó¦
C£®̉×ÈÜÓÚË® D£®µÈÖÊÁ¿µÄWÓë±½·Ö±đÍêȫȼÉƠ£¬Ç°ƠßÏûºÄµÄÑơÆø¶à
4£®WÓĐ̉»ÖÖ·¼Ïă×åµÄͬ·Ö̉́¹¹̀壬¸ĂÎïÖÊÄÜÔÚ̉»¶῭ơ¼₫Ï·¢Éú¾ÛºÏ·´Ó¦£¬ÏàÓ¦µÄ»¯Ñ§·½³̀ʽΪ ¡£
£¨ 8·Ö£© ̉ÑÖª£ºÔÚ298K¡¢100kPaʱ£¬
¢ÙC(s,ʯī)£«O2(g) = CO2(g) ¡÷H1 = £400 kJ¡¤mol£1£»
¢Ú2H2(g)£«O2(g) = 2H2O(l) ¡÷H2 = £570 kJ¡¤mol£1£»
¢Û2C2H2(g)£«5O2(g) = 4CO2(g)+ 2H2O(l) ¡÷H3 = £2600 kJ¡¤mol£1£»
£¨1£©Đ´³ö298KʱÓÉC(s,ʯī)ºÍH2(g)Éú³É1 mol C2H2(g)·´Ó¦µÄÈÈ»¯Ñ§·½³̀ʽ ¡£
£¨2£©ÏÖÓĐ̉»¶¨Á¿µÄ̉̉ȲÔÚ×ăÁ¿ÑơÆøÖĐÍêȫȼÉƠ£¬·Å³öÈÈÁ¿650 kJ¡£½«·´Ó¦ºóµÄ¶₫Ñơ»¯̀¼Æø̀建»ºÍ¨Èëµ½º¬ÓĐ0.5 mol Ca (OH)2µÄ³ÎÇåʯ»̉Ë®ÖĐ³ä·Ö·´Ó¦¡£ËùµĂÈÜ̉ºÎª ¡£
½«·´Ó¦ºóµÄÈÜ̉º·ÖΪa¡¢bÁ½µÈ·Ư£¬·Ö±đ½øĐĐÏÂÁĐʵÑ飬»Ø´đÏàÓ¦ÎỀ⣺
¢ÙÔÚaÖĐ¼ÓÈëÉÙÁ¿µÄÇâÑơ»¯ÄÆÈÜ̉º£¬Đ´³ö·´Ó¦µÄÀë×Ó·½³̀ʽ ¡£
¢Ú¼ÓÈÈb£¬¹Û²́µ½ ¡£
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com