
题目列表(包括答案和解析)
将总物质的量为m mol的Na2O2和NaHCO3的混合物在密闭容器中加热至2.50℃,使其充分反应,NaHCO3在混合物中的物质的量分数为x。
(1)当x=l/2时,容器中固体产物 (写化学式),其物质的量为 。
(2)若反应后生成的气体为O2和H2O,则x的取值范围 。
(3)当0<x<l/3时,产生气体的物质的量n与x的数学表达式 (写化学式)。
(12分)某化学研究性学习小组对某Na2CO3和NaHCO3的混合溶液(以下简称“样品溶液”)的组成进行探究。请按要求完成下列研究报告。
[资料获悉]36.5%的浓盐酸的密度为1.19 g·cm-3。
[探究思路]用1.00 mol·L-1的稀盐酸测定样品溶液的组成。
[实验探究]用36.5%的浓盐酸配制100 mL 1.00 mol·L-1的稀盐酸需要的玻璃仪器有烧杯、玻璃棒、量筒、 。
取20.0 mL样品溶液不断加入1.00 mol·L-1的稀盐酸,加入盐酸的体积和产生的现象见下表。
|
反应阶段 |
I |
II |
III |
|
盐酸体积x/ mL |
0<x≤10.0 |
10.0<x≤40.0 |
x>40.0 |
|
现 象 |
无气体 |
有气体 |
无气体 |
第I阶段溶液中反应的离子方程式为: 。
样品溶液中c(CO32-)= 。
[交流讨论]
(1)如果将2.85 g 某Na2CO3和NaHCO3的固体混合物溶于水制成溶液,然后逐滴加入1.00 mol·L-1的稀盐酸并充分反应,若第I阶段消耗盐酸的体积为15.0 mL,当滴加到45.0 mL时,反应的第II阶段结束。则此Na2CO3和NaHCO3的混合物中Na2CO3的质量分数为 。
(2)有同学认为,测定Na2CO3和NaHCO3固体混合物中Na2CO3的质量分数,完全不必将混合物配制成溶液,也不必要使用其他反应试剂,即可达到目的,则此时实验的主要操作方法的名称是称量和 ,在实验中需要测定的数据有 。
将总物质的量为m mol的Na2O2和NaHCO3的混合物在密闭容器中加热至2.50℃,使其充分反应,NaHCO3在混合物中的物质的量分数为x。
(1)当x=l/2时,容器中固体产物 (写化学式),其物质的量为 。
(2)若反应后生成的气体为O2和H2O,则x的取值范围 。
(3)当0<x<l/3时,产生气体的物质的量n与x的数学表达式 (写化学式)。
将总物质的量为n mol的钠和铝(其中钠的物质的量分数为x),投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V L。下列关系式中正确的是( )
A.x=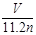 B.0 < x ≤ 0.5
B.0 < x ≤ 0.5
C.V=33.6n(1-x) D.11.2n < V ≤ 22.4n
(12分)某化学研究性学习小组对某Na2CO3和NaHCO3的混合溶液(以下简称“样品溶液”)的组成进行探究。请按要求完成下列研究报告。
[资料获悉]36.5%的浓盐酸的密度为1.19 g·cm-3。
[探究思路]用1.00mol·L-1的稀盐酸测定样品溶液的组成。
[实验探究]用36.5%的浓盐酸配制100 mL 1.00 mol·L-1的稀盐酸需要的玻璃仪器有烧杯、玻璃棒、量筒、 。
取20.0 mL样品溶液不断加入1.00 mol·L-1的稀盐酸,加入盐酸的体积和产生的现象见下表。
| 反应阶段 | I | II | III |
| 盐酸体积x/ mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现 象 | 无气体 | 有气体 | 无气体 |
第I阶段溶液中反应的离子方程式为: 。
样品溶液中c(CO32-)= 。
[交流讨论]
(1)如果将2.85 g 某Na2CO3和NaHCO3的固体混合物溶于水制成溶液,然后逐滴加入1.00 mol·L-1的稀盐酸并充分反应,若第I阶段消耗盐酸的体积为15.0 mL,当滴加到45.0 mL时,反应的第II阶段结束。则此Na2CO3和NaHCO3的混合物中Na2CO3的质量分数为 。
(2)有同学认为,测定Na2CO3和NaHCO3固体混合物中Na2CO3的质量分数,完全不必将混合物配制成溶液,也不必要使用其他反应试剂,即可达到目的,则此时实验的主要操作方法的名称是称量和 ,在实验中需要测定的数据有 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com