
题目列表(包括答案和解析)
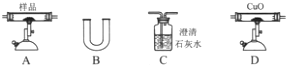 (2012?昆明模拟)选用如下装置对草酸钙晶体(CaC2O4?H2O)的分解产物进行研究.
(2012?昆明模拟)选用如下装置对草酸钙晶体(CaC2O4?H2O)的分解产物进行研究.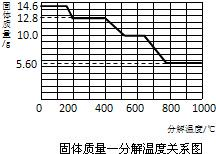
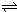 2H2(g)+O2(g)△H=+484kJ?mol-1;测得20min时O2的物质的量为0.0016mol,则前20min的反应速率v(H2O)=
2H2(g)+O2(g)△H=+484kJ?mol-1;测得20min时O2的物质的量为0.0016mol,则前20min的反应速率v(H2O)=| c2(H2)?c(O2) |
| c2(H2O) |
| c2(H2)?c(O2) |
| c2(H2O) |
(11分)2005年的诺贝尔化学奖颁给了3位在烯烃复分解反应研究方面做出突出贡献的化学家。烯烃复分解反应实际上是在金属烯烃络合物的催化下实现C=C双键两边基团换位的反应。如下图表示了两个丙烯分子进行烯烃换位,生成两个新的烯烃分子——丁烯和乙烯。
现以石油裂解得到的丙烯为原料,经过下列反应可以分别合成重要的化工原料I和G。I和G在不同条件下反应可生成多种化工产品,如环酯J。
请按要求填空:
(1)写出下列反应的反应类型:①:_________,⑥:__________,⑧:_____________
(2)反应②的化学方程式是___________________________________________。
(3)反应④、⑤中有一反应是与HCl加成,该反应是________(填反应编号),设计这一步反应的目的是 ,物质E的结构简式是_______________。
(4)反应⑩的化学方程式是___________________________________________。
(共8分)
(1)(3分)有反应:2NO2 N2O4 △H<0,根据图像判断后填空:
N2O4 △H<0,根据图像判断后填空:
|
 t1 t2 t3 t4 t5 t6 t
t1 t2 t3 t4 t5 t6 t
2005年10月5日,瑞典皇家科学院将本年度诺贝尔化学奖授予法国化学家伊夫·肖万和两位美国化学家罗伯特·格拉布和理查德·施罗克,以表彰他们在烯烃复分解反应研究和应用方面做出的卓越贡献。


伊夫·肖万 罗伯特·格拉布 理查德·施罗克
烯烃复分解反应实际上是在金属烯烃络合物的催化下实现C=C双键两边基团换位的反应。如下图表示了两个丙烯分子进行烯烃换位,生成两个新的烯烃分子——2-丁烯和乙烯:
现以石油裂解得到的丙烯为原料,经过下列反应可以分别合成重要的化工原料I和G。I和G在不同条件下反应可生成多种化工产品,如环酯J。
请按要求填空:
(1)写出下列反应的反应类型:
③: ,⑥: ,⑧: 。
(2)反应②的化学方程式是: 。
(3)反应④、⑤中有一反应是与HCl加成,该反应是 (填反应编号),设计这一步反应的目的是 ;物质E的结构简式是 。
(4)反应⑩的化学方程式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com