
题目列表(包括答案和解析)
高锰酸钾俗称PP粉,为强氧化剂,遇到有机物就放出活性氧。这种氧有杀灭细菌的作用,且杀菌能力极强。某学生欲在实验室配制1 L 0.06 mol/L KMnO4稀溶液,用来清洗伤口。
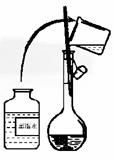
(1)实验过程中需用托盘天平称取KMnO4晶体的质量为__________g。
(2)其操作步骤如下图所示,则右图所示操作应在下图中__________(填选项字母)之间。
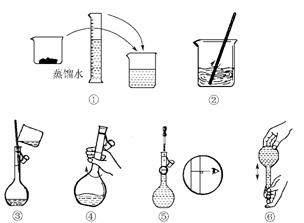
A.②与③ B.①与② C.④与⑤
(3)若该同学在配制溶液时,进行了如下操作,其中使所配溶液浓度偏低的操作有__________(填选项字母)。
A.称量KMnO4晶体时,指针偏向右边
B.将KMnO4晶体放在烧杯中溶解,冷却后,转移至含有少量蒸馏水的容量瓶中
C.定容时,仰视刻度线
D.振荡摇匀后,发现溶液液面低于刻度线,再滴加少量蒸馏水至刻度线处
高锰酸钾在不同的条件下发生还原反应如下:
MnO4- +5e + 8H+ → Mn2+ + 4H2O
MnO4- +3e +2H2O → MnO2↓+4OH-
MnO4- + e → MnO42-(溶液绿色)
(1)从上述三个半反应中可以看出高锰酸根离子还原产物受到溶液的 影响。
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为 → 。
(3)将PbO2投入到MnSO4酸性溶液中搅拌溶液变为紫红色。下列说法正确的是( )。
a.氧化性:PbO2>KMnO4 b.还原性:PbO2>KMnO4 c.该反应可以用盐酸酸化
(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量比为3:2。完成下列化学方程式,并标出电子转移的方向和数目。
KMnO4+ K2S + → K2MnO4 + K2SO4+ S↓+
若生成5.44g单质硫,反应过程中转移的电子数约为 ;若反应中有22mol电子转移,则生成K2SO4和S的物质的量比为 。
高锰酸钾在不同的条件下发生还原反应如下:
MnO4- + 5e + 8H+ → Mn2+ + 4H2O
MnO4- +3e + 2H2O → MnO2↓+ 4OH-
MnO4- + e → MnO42- (溶液绿色)
(1)从上述三个半反应中可以看出高锰酸根离子还原产物受到溶液的 影响。
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为 → 。
(3)将PbO2投入到MnSO4酸性溶液中搅拌溶液变为紫红色。下列说法正确的是( )。
a.氧化性:PbO2>KMnO4 b.还原性:PbO2>KMnO4 c.该反应可以用盐酸酸化
(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量比为3:2。完成下列化学方程式,并标出电子转移的方向和数目。
KMnO4 + K2S + → K2MnO4 + K2SO4+ S↓+
若生成5.44g单质硫,反应过程中转移的电子数约为 ;若反应中有22mol电子转移,则生成K2SO4和S的物质的量比为 。
(1)向含有酚酞的氢氧化钠溶液中滴加双氧水,溶液由红色褪至无色,主要原因是双氧水具有______________性。
(2)将双氧水加入经酸化的高锰酸钾溶液中,溶液的紫红色褪去,此时双氧水表现出______________性。
(3)久置的油画,白色部位(PbSO4)常会变黑(PbS),用双氧水抹擦后又可恢复原貌,有关反应的化学方程式为:
PbS+4H2O2![]() PbSO4+4H2O
PbSO4+4H2O
此时双氧水表现出______________性。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com