
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
”…»έ―ΈΒγΫβΖ®ΜώΒΟΒΡ¥÷¬ΝΚ§”–“ΜΕ®ΝΩΒΡΫπ τΡΤΚΆ«βΤχΘ§’β–©‘”÷ Ω…≤…”Ο¥ΒΤχΨΪΝΕΖ®≥ΐ»ΞΘ§≤ζ…ζΒΡΈ≤ΤχΨ≠¥ΠάμΚσΩ…”ΟΗ÷≤ΡΕΤ¬ΝΓΘΙΛ“’Νς≥Χ»γœ¬ΘΚ
Θ®ΉΔΘΚNaCl»έΒψΈΣ801ΓφΘΜAlCl3‘Ύ181Γφ…ΐΜΣΘ©
Θ®1Θ©ΨΪΝΕ«ΑΘ§–η«ε≥ΐέαέω±μΟφΒΡ―θΜ·ΧζΚΆ ·”Δ…ΑΘ§Ζά÷ΙΨΪΝΕ ±ΥϋΟ«Ζ÷±π”κ¬ΝΖΔ…ζ÷ΟΜΜΖ¥”Π≤ζ…ζ–¬ΒΡ‘”÷ Θ§œύΙΊΒΡΜ·―ßΖΫ≥Χ ΫΈΣΔΌ ΚΆΔΎ ΓΘ
Θ®2Θ©ΫΪCl2Ν§–χΆ®»κέαέω÷–ΒΡ¥÷¬Ν»έΧεΘ§‘”÷ ΥφΤχ≈ί…œΗΓ≥ΐ»ΞΓΘΤχ≈ίΒΡ÷ς“Σ≥…Ζ÷≥ΐCl2ΆβΜΙΚ§”– ΘΜΙΧΧ§‘”÷ ’≥ΗΫ”ΎΤχ≈ί…œΘ§‘Ύ»έΧε±μΟφ–Έ≥…ΗΓ‘ϋΘ§ΗΓ‘ϋ÷–ΩœΕ®¥φ‘Ύ
Θ®3Θ©‘Ύ”ΟΖœΦν“Κ¥ΠάμAΒΡΙΐ≥Χ÷–Θ§ΥυΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ ΓΘ
Θ®4Θ©Η÷≤ΡΕΤ¬ΝΚσΘ§±μΟφ–Έ≥…ΒΡ÷¬Οή―θΜ·¬ΝΡΛΡήΖά÷ΙΗ÷≤ΡΗ· ¥Θ§Τδ‘≠“ρ « ΓΘ
”…»έ―ΈΒγΫβΖ®ΜώΒΟΒΡ¥÷¬ΝΚ§”–“ΜΕ®ΝΩΒΡΫπ τΡΤΚΆ«βΤχΘ§’β–©‘”÷ Ω…≤…”Ο¥ΒΤχΨΪΝΕΖ®≥ω»ΞΘ§≤ζ…ζΒΡΈ≤ΤχΨ≠¥ΠάμΚσΩ…”Ο”ΎΗ’≤≈ΕΤ¬ΝΓΘΙΛ“’Νς≥Χ»γœ¬ΘΚ
Θ®ΉΔΘΚNaCl»έΒψΈΣ801ΓφΘΜAlCl3‘Ύ181Γφ…ΐΜΣΘ©
Θ®1Θ©ΨΪΝΕ«ΑΘ§–η«ε≥ΐέαέω±μΟφΒΡ―θΜ·ΧζΚΆ ·”Δ…ΑΘ§Ζά÷ΙΨΪΝΕ ±ΥϋΟ«Ζ÷±π”κ¬ΝΖΔ…ζ÷ΟΜΜΖ¥”Π≤ζ…ζ–¬ΒΡ‘”÷ Θ§œύΙΊΒΡΜ·―ßΖΫ≥Χ ΫΈΣΔΌ ΚΆΔΎ
Θ®2Θ©ΫΪCl2Ν§–χΆ®»κέαέω÷–ΒΡ¥÷¬Ν»έΧεΘ§‘”÷ ΥφΤχ≈ί…œΗΓ≥ΐ»ΞΓΘΤχ≈ίΒΡ÷ς“Σ≥…Ζ÷≥ΐCl2ΆβΜΙΚ§”– ΘΜΙΧΧ§‘”÷ ’≥ΗΫ”ΎΤχ≈ί…œΘ§‘Ύ»έΧε±μΟφ–Έ≥…ΗΓ‘ϋΘ§ΗΓ‘ϋ÷–ΩœΕ®¥φ‘Ύ
Θ®3Θ©‘Ύ”ΟΖœΦν“Κ¥ΠάμAΒΡΙΐ≥Χ÷–Θ§ΥυΖΔ…ζΖ¥”ΠΒΡάΐΉ”ΖΫ≥Χ ΫΈΣ
Θ®4Θ©ΕΤ¬ΝΒγΫβ≥Ί÷–Θ§Ϋπ τ¬ΝΈΣ ΦΪΘ§»έ»Ύ―ΈΒγΕΤ÷–¬Ν‘ΣΥΊΚΆ¬»‘ΣΥΊ÷ς“Σ“‘AlCl4®DΚΆAl2Cl7®D–Έ Ϋ¥φ‘ΎΘ§¬ΝΒγΕΤΒΡ÷ς“ΣΒγΦΪΖ¥”Π ΫΈΣ
Θ®5Θ©Η÷≤ΡΕΤ¬ΝΚσΘ§±μΟφ–Έ≥…ΒΡ÷¬Οή―θΜ·¬ΝΡΛΡήΖά÷ΙΗ÷≤ΡΗ· ¥Θ§Τδ‘≠“ρ «
”…”ΎFe(OH)2ΦΪ“Ή±Μ―θΜ·Θ§Υυ“‘ Β―ι “ΚήΡ―”Ο―«Χζ―Έ»ή“Κ”κ…’Φν»ή“ΚΖ¥”Π÷ΤΒΟFe(OH)2ΑΉ…Ϊ≥ΝΒμΓΘ»τ”Οœ¬ΆΦΥυ Ψ Β―ιΉΑ÷ΟΘ§‘ρΩ…÷ΤΒΟ¥ΩΨΜΒΡFe(OH)2ΑΉ…Ϊ≥ΝΒμΓΘ“―÷ΣΝΫΦΪ≤ΡΝœΖ÷±πΈΣ ·ΡΪΚΆΧζΘΚ
Θ®1Θ©aΦΪ≤ΡΝœΈΣ Θ§aΒγΦΪΖ¥”Π ΫΈΣ ΓΘ
Θ®2Θ©ΒγΫβ“ΚdΩ…“‘ « Θ§‘ρΑΉ…Ϊ≥ΝΒμ‘ΎΒγΦΪ…œ…ζ≥…ΘΜΒγΫβ“Κd“≤Ω…“‘ « Θ§‘ρΑΉ…Ϊ≥ΝΒμ‘ΎΝΫΦΪΦδΒΡ»ή“Κ÷–…ζ≥…ΓΘ
AΘ°¥ΩΥ° BΘ°NaCl»ή“Κ CΘ°NaOH»ή“Κ DΘ°CuCl2»ή“Κ
Θ®3Θ©“ΚΧεcΈΣ±ΫΘ§ΤδΉς”Ο « Θ§‘ΎΦ”±Ϋ÷°«ΑΕ‘d»ή“ΚΫχ––Φ”»»÷σΖ–¥ΠάμΘ§ΡΩΒΡ « ΓΘ
Θ®4Θ©ΈΣΝΥ‘ΎΕΧ ±ΦδΡΎΩ¥ΒΫΑΉ…Ϊ≥ΝΒμΘ§Ω…“‘≤…»ΓΒΡ¥κ © « ΓΘ
AΘ°ΗΡ”ΟH2SO4ΉςΒγΫβ“Κ BΘ° Β±‘ω¥σΒγ‘¥Βγ―Ι
CΘ° Β±Υθ–ΓΝΫΦΪΦδΨύάκ DΘ° Β±ΒΊΫΒΒΆΒγΫβ“ΚΒΡΈ¬Ε»
Θ®5Θ©»τdΗΡΈΣNa2SO4»ή“ΚΘ§Β±ΒγΫβ“ΜΕΈ ±ΦδΘ§Ω¥ΒΫΑΉ…Ϊ≥ΝΒμΚσΘ§‘ΌΖ¥Ϋ”Βγ‘¥ΦΧ–χΒγΫβΘ§≥ΐΝΥΒγΦΪ
…œΩ¥ΒΫΒΡΤχ≈ίΆβΘ§Νμ“ΜΟςœ‘ΒΡœ÷œσΈΣ ΓΘ
Θ®6Ζ÷Θ©”…”ΎΈ¬ “–ß”ΠΚΆΉ ‘¥ΕΧ»±Β»Έ ΧβΘ§»γΚΈΫΒΒΆ¥σΤχ÷–ΒΡCO2Κ§ΝΩ≤ΔΦ”“‘ΩΣΖΔάϊ”ΟΘ§“ΐΤπΝΥΗςΙζΒΡΤ’±ι÷Ί ”ΓΘΡΩ«ΑΙΛ“Β…œ”–“Μ÷÷ΖΫΖ® «”ΟCO2…ζ≤ζ»ΦΝœΦΉ¥ΦΓΘ“ΜΕ®ΧθΦΰœ¬ΖΔ…ζΖ¥”ΠΘΚCO2(g)+3H2(g) CH3OH(g)+H2O(g)Θ§”“ΆΦ±μ ΨΗΟΖ¥”ΠΫχ––Ιΐ≥Χ÷–ΡήΝΩΒΡ±δΜ·ΓΘ
CH3OH(g)+H2O(g)Θ§”“ΆΦ±μ ΨΗΟΖ¥”ΠΫχ––Ιΐ≥Χ÷–ΡήΝΩΒΡ±δΜ·ΓΘ
(1)ΙΊ”ΎΗΟΖ¥”ΠΒΡœ¬Ν–ΥΒΖ®÷–Θ§’ΐ»ΖΒΡ «_______ΓΘ
| AΘ°ΓςH>0Θ§ΓςS>0ΘΜ | BΘ°ΓςH>0Θ§ΓςS<0ΘΜ | CΘ°ΓςH<0Θ§ΓςS<0ΘΜ | DΘ°ΓςH<0Θ§ΓςS>0ΓΘ |
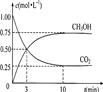
”…”ΎΈ¬ “–ß”ΠΚΆΉ ‘¥ΕΧ»±Β»Έ ΧβΘ§»γΚΈΫΒΒΆ¥σΤχ÷–ΒΡCO2Κ§ΝΩ≤ΔΦ”“‘ΩΣΖΔάϊ”ΟΘ§“ΐΤπΝΥΗςΙζΒΡΤ’±ι÷Ί ”ΓΘ
Θ®1Θ©ΡΩ«ΑΘ§”Ο≥§ΝΌΫγCO2Θ®ΤδΉ¥Χ§Ϋι”ΎΤχΧ§ΚΆ“ΚΧ§÷°ΦδΘ©¥ζΧφΖζάϊΑΚΉςάδΦΝ“―≥…ΈΣ“Μ÷÷«ς ΤΘ§’β“ΜΉωΖ®Ε‘ΜΖΨ≥ΒΡΜΐΦΪ“β“ε‘Ύ”Ύ ΓΘ
Θ®2Θ©ΫΪCO2ΉΣΜ·≥…”–ΜζΈοΩ…”––ß Βœ÷ΧΦ―≠ΜΖΓΘCO2ΉΣΜ·≥…”–ΜζΈοΒΡάΐΉ”ΚήΕύΘ§»γΘΚ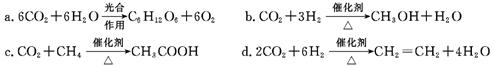
“‘…œΖ¥”Π÷–Θ§‘≠Ή”άϊ”Ο¬ ΉνΗΏΒΡ « ΓΘ
Θ®3Θ©»τ”–4.4g CO2”κΉψΝΩH2«ΓΚΟΆξ»ΪΖ¥”ΠΘ§…ζ≥…“ΚΧ§ΦΉ¥ΦΚΆΤχΧ§Υ°Θ§Ω…Ζ≈≥ω4.9 kJΒΡ»»ΝΩΘ§ ‘–¥≥ωΗΟΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ Ϋ_______________________________________ΓΘ
Θ®4Θ©ΈΣΧΫΨΩ”ΟCO2ά¥…ζ≤ζ»ΦΝœΦΉ¥ΦΒΡΖ¥”Π‘≠άμΘ§œ÷Ϋχ––»γœ¬ Β―ιΘΚ‘Ύ“ΜΚψΈ¬Κψ»ίΟή±’»ίΤςΘ§≥δ»Υ1mol CO2ΚΆ3molH2Θ§Ϋχ––Ζ¥”ΠΓΘ≤βΒΟCO2ΚΆCH3OH(g)ΒΡ≈®Ε»Υφ ±Φδ±δΜ·»γΆΦΥυ ΨΓΘ
¥”Ζ¥”ΠΩΣ ΦΒΫΤΫΚβv(H2)= _____________ΘΜΗΟΈ¬Ε»œ¬ΒΡΤΫΚβ≥Θ ΐ ΐ÷Β=__________ΓΘ
Θ®5Θ©CO2‘ΎΉ‘»ΜΫγ―≠ΜΖ ±Ω…”κCaCO3Ζ¥”ΠΓΘCaCO3 «“Μ÷÷Ρ―»ήΈο÷ Θ§ΤδKsp="=" 2.8ΓΝ10Θ≠9ΓΘCaCl2»ή“Κ”κNa2CO3»ή“ΚΜλΚœΩ…–Έ≥…CaCO3≥ΝΒμΘ§œ÷ΫΪ4ΓΝ10Θ≠4mol/L Na2CO3»ή“Κ”κΡ≥≈®Ε»ΒΡCaCl2»ή“ΚΒ»ΧεΜΐΜλΚœΘ§‘ρ…ζ≥…≥ΝΒμΥυ–ηCaCl2»ή“ΚΒΡΉν–Γ≈®Ε»ΈΣ______________ΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com