
题目列表(包括答案和解析)
(7分) 右图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。

(1)图中的两处明显的错误是
① ;② 。
(2)A仪器的名称是____________,
B仪器的名称是_______________。
(3)实验时A中除加入少量自来水外,为防止 液体暴沸还需加入少量_______。
(7分) 右图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。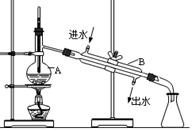
(1)图中的两处明显的错误是
① ;② 。
(2)A仪器的名称是____________,
B仪器的名称是_______________。
(3)实验时A中除加入少量自来水外,为防止 液体暴沸还需加入少量_______。
(7分)右图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。
(1)图中的两处明显的错误是
① ;② 。
(2)A仪器的名称是____________,
B仪器的名称是_______________。
(3)实验时A中除加入少量自来水外,为防止 液体暴沸还需加入少量_______。
(l2分)下表是元素周期表的一部分,根据所给的10 种元素,回答下列
问题。
(1)非金属性最强的元素是 ;
(2)Ne 原子结构示意图为 ;
(3)C 与N 中,原子半径较小的是 ;
(4)氯水具有漂白作用,是由于其中含有 (填“HCl”或“HClO”)
(5)元素最高价氧化物对应的水化物中,碱性最强的是 (填化学式),呈两性的是 (填化学式);
(6)元素硅的氧化物常用于制造 (填一种高性能的现代通讯材料的
名称);
(7)右图 为某有机物的球棍模型(其中
为某有机物的球棍模型(其中 代表氢原子代表
代表氢原子代表 碳原子),该有机物中碳元素与氢元素的质量比m(C):m(H)= 。(相对原子质量C-12、H-l)
碳原子),该有机物中碳元素与氢元素的质量比m(C):m(H)= 。(相对原子质量C-12、H-l)
(8)镁是制造汽车、飞机、火箭的重要材料。写出工业上电解熔融氯化镁获得金属镁的化学方程式 。
(10分)右图是用铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。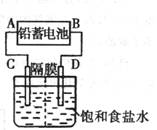
已知:铅蓄电池在放电时发生下列电极反应
负极:![]()
正极:![]()
(1)请写出电解饱和食盐水的化学方程式 ;
(2)若在电解池中C极一侧滴2滴酚酞试液、电解一段时间后,未呈红色,说明蓄电池的A极为 极
(3)用铅蓄电池电解1 L饱和食盐水(食盐水足量、密度为1.15 g/cm3)时:
①若收集到11.2 L(标准状况下)氯气,则至少转移电子 mol。
②若蓄电池消耗H2SO4 2 mol,则可收集到H2的体积(标准状况下)为 L。
③若消耗硫酸![]() mol,电解后除去隔膜,所得溶液中NaOH的质量分数表达式为(假设氯气全部排出) (用含
mol,电解后除去隔膜,所得溶液中NaOH的质量分数表达式为(假设氯气全部排出) (用含![]() 的代数式表达)。
的代数式表达)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com