
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
аТаЭВФСЯФЩУзМЖFeЗлОпгаГЌЧПЕФДХадЃЌФмгУзїИпУмЖШДХМЧТМЕФНщжЪвдМАИпаЇ? ДпЛЏМСЕШЁЃ
IЃЎЪЕбщЪвВЩгУЦјЯрЛЙдЗЈжЦБИФЩУзМЖFe,ЦфСїГЬШчЯТЃК

ЃЈ1ЃЉ ЙЬЬхМгШШЭбЫЎЭЈГЃвЊЭЈШы????????????????????????????????????? ЁЃ
ЙЬЬхМгШШЭбЫЎЭЈГЃвЊЭЈШы????????????????????????????????????? ЁЃ
ЃЈ2ЃЉЩњГЩФЩУзМЖFeЕФЛЏбЇЗНГЬЪНЮЊ????????????????????????????????????????????? ЁЃ
ЂђЃЎдкВЛЭЌЮТЖШЯТЃЌФЩУзМЖFeЗлгыЫЎеєЦјЗДгІЕФЙЬЬхВњЮяВЛЭЌЃКЮТЖШЕЭгк570ЁцЪБЩњГЩFeOЃЌИпгк570ЁцЪБЩњГЩ ЁЃМзЭЌбЇгУЯТЭМЫљЪОзАжУНјааФЩУзМЖFeЗлгыЫЎеєЦјЕФЗДгІВЂбщжЄЙЬЬхВњЮяЁЃ
ЁЃМзЭЌбЇгУЯТЭМЫљЪОзАжУНјааФЩУзМЖFeЗлгыЫЎеєЦјЕФЗДгІВЂбщжЄЙЬЬхВњЮяЁЃ

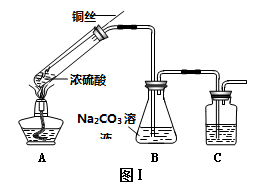
ЃЈ3ЃЉBжаЪеМЏЕНЕФЦјЬхЪЧ?????????????? (ЬюУћГЦ)ЃЌCзАжУЕФзїгУЪЧ????????? ЁЃ
ЃЈ4ЃЉввЭЌбЇЮЊЬНОПЪЕбщНсЪјКѓЪдЙмФкЕФЙЬЬхЮяжЪГЩЗжЃЌНјааСЫЯТСаЪЕбщЃК

ввЭЌбЇШЯЮЊИУЬѕМўЯТЗДгІЕФЙЬЬхВњЮяЮЊFeOЁЃБћЭЌбЇШЯЮЊИУНсТлВЛе§ШЗЃЌЫћЕФРэгЩЪЧ????????????????? (гУРызгЗНГЬЪНБэЪО)ЁЃ
ЃЈ5ЃЉЖЁЭЌбЇГЦШЁ5ЃЎ60gFeЗлЃЌЗДгІвЛЖЮЪБМфКѓЃЌЭЃжЙМгШШЁЃНЋЪдЙмФкЕФЙЬЬхЮяжЪдкИЩдяЦїжаРфШДКѓЃЌГЦЕУжЪСПЮЊ6ЃЎ88gЁЃШЛКѓНЋРфШДКѓЕФЙЬЬхЮяжЪгызуСПFeCl3ШмвКГфЗжЗДгІЃЌЯћКФ0ЃЎ08molFeCl3ЁЃЖЁЭЌбЇЪЕбщЕФЙЬЬхВњЮяЮЊ??????????????????????? ЁЃ

| бЁЯю | ЪЕбщВйзї | ЪЕбщФПЕФЛђНсТл |
| A | НЋФГМибЮШмгкбЮЫсКѓВњЩњФмЪЙГЮЧхЪЏЛвЫЎБфЛызЧЕФЮоЩЋЮоЮЖЕФЦјЬх | ЫЕУїИУМибЮЪЧK2CO3 |
| B | ЯђКЌгаЩйСПFeCl3ЕФCuCl2ШмвКжаМгШызуСПCuЗлЃЌНСАшвЛЖЮЪБМфКѓЙ§ТЫ | Г§ШЅCuCl2ШмвКжаЕФЩйСПFeCl3ЃЌЬсДПCuCl2ШмвК |
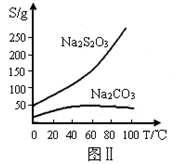
| C | ГЃЮТЯТЃЌЯђБЅКЭNa2CO3ШмвКжаЭЈШыЙ§СПCO2ЃЌШмвКБфЛызЧ | ЫЕУїГЃЮТЯТNaHCO3ЕФШмНтЖШПЩФмБШNa2CO3ЕФШмНтЖШаЁ |
| D | C2H5OHгыХЈСђЫсдк170ЁцЙВШШЃЌНЋжЦЕУЕФЦјЬхжБНгЭЈШыЫсадKMnO4ШмвКжа | МьбщжЦЕУЦјЬхЪЧЗёЮЊввЯЉ |

| ||
| ||
| ||
| ||
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com