
题目列表(包括答案和解析)
(1)请完成制取溴乙烷的化学方程式:______________________________。
若按烧瓶内液体的体积不小于烧瓶容积的1/3,不大于烧瓶容积的2/3,则反应装置中烧瓶的容积最合适的是_________。
A.50 mL B.100 mL C.150 mL D.250 mL
(2)用下图仪器安装反应装置,要求达到减少反应物损失、防止环境污染的目的,有关仪器连接顺序为_________ (填数字)。
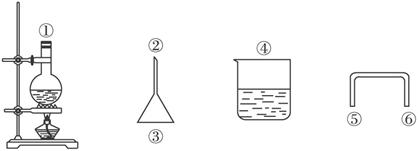
(3)反应过程中,可能发生的副反应为(至少填两个):
_____________________________________________________________________,_____________________________________________________________________。
(4)实验结果从反应混合物中分离出粗制黄色的溴乙烷,产生黄色的主要原因是其含有____________(填化学式)。欲得到无色的溴乙烷的方法是_______________(填试剂和操作名称)。
(5)本实验的理论产量为____________g。
(1)请完成制取溴乙烷的化学方程式:______________________________________。
若按烧瓶内液体的体积不小于烧瓶容积的1/3,不大于烧瓶容积的2/3,则反应装置中烧瓶的容积最合适的是____________。
A.50 mL B.100 mL C.150 mL D.250 mL
(2)用下图仪器安装反应装置,要求达到减少反应物损失、防止环境污染的目的,有关仪器连接顺序为______________(填数字)。
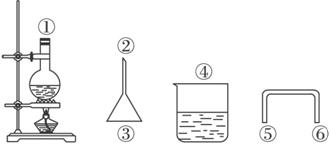
(3)反应过程中,可能发生的副反应为(至少填两个):_________________________________。
(4)实验结果从反应混合物中分离出粗制黄色的溴乙烷,产生黄色的主要原因是其含有______________(填化学式)。欲得到无色的溴乙烷的方法是用______________吸收(填试剂和操作名称)。
(5)本实验的理论产量为______________g。
(一)(2分)下列实验操作不正确的是 _。
A.在催化剂存在的条件下, 苯和溴水发生反应可生成无色、比水重的液体溴苯
B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,
完成乙醇氧化为乙醛的实验
C.醇中含有少量水可加入硫酸铜再蒸馏制得无水乙醇
D.试管中先加入一定量浓硫酸,再依次加入适量浓硝酸、苯,然后加热制取硝基苯
E.实验室制取乙烯时,放入几片碎瓷片,以避免混合液在受热沸腾时剧烈跳动
F.配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀
刚好溶解为止
G.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、
待液体分层后,滴加硝酸银溶液
(二)(8分)
乙醇的沸点是78℃,能与水以任意比混溶。乙醚的沸点为34.6℃,难溶于水,在饱和Na2CO3 溶液中几乎不溶,乙醚极易燃烧。实验室制醚的反应原理是:
2CH3CH2OH ![]() H2O + CH3CH2—O—CH2CH?3 (乙醚)
H2O + CH3CH2—O—CH2CH?3 (乙醚)
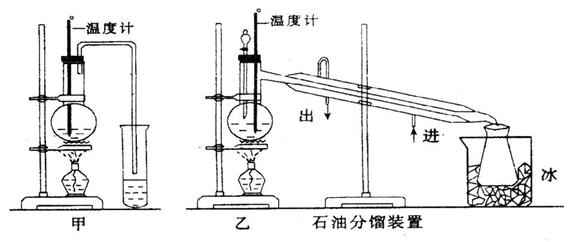
(1)甲图和乙图是两套实验室制乙醚的装置,选装置_________(填“甲”或“乙”)最合理,理由是_____________________________________。
(2)反应中温度计的正确位置是水银球置于____________________。
(3)用装置乙制得的乙醚中可能含有大量的杂质,该杂质是__________,
除去这种杂质的简易方法是__________________
(4)如果温度太高,将会发生副反应,产物为____________________
完成下列反应方程式
(1)乙醇与金属钠反应
(2)乙烯和溴的四氯化碳溶液反应
(3)苯乙烯一定条件下生成聚苯乙烯
(4)甲苯与浓硝酸、浓硫酸的混合酸在100℃下的反应
完成下列反应方程式
(1)乙醇与金属钠反应
(2)乙烯和溴的四氯化碳溶液反应
(3)苯乙烯一定条件下生成聚苯乙烯
(4)甲苯与浓硝酸、浓硫酸的混合酸在100℃下的反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com