
题目列表(包括答案和解析)
①O3:_______________________________________________________________。
②Na2O2:_____________________________________________________________。
③Na2O:______________________________________________________________。
(2)指出氧元素在下列各物质中的化合价:
O3____________________;K2O2__________________;Na2O__________________________。
(3)RbO2也能吸收CO2放出氧气,其化学方程式是__________________________________。
(4)人体内O-2(超氧离子)对健康有害,使人过早衰老,但在催化剂SOD存在下可发生如下反应,请完成该反应的离子方程式:
![]() O-2+
O-2+ ![]() H2O
H2O![]()
![]() H2O2+
H2O2+![]() O2↑+
O2↑+![]()
![]()
4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g);ΔH=-905 kJ·mol-1
4NO(g)+6H2O(g);ΔH=-905 kJ·mol-1
2H2(g)+O2(g)![]() 2H2O;ΔH=-483.6 kJ·mol-1
2H2O;ΔH=-483.6 kJ·mol-1
则N2(g)+3H2(g)![]() 2NH3(g)的ΔH=________。
2NH3(g)的ΔH=________。
(2)工业上在一定温度下,将一定量的N2和H2通入到体积为
①增大压强②增大反应物的浓度③使用催化剂④降低温度
(3)当化学反应N2(g)+2H2(g) ![]() 2NH3(g)达到平衡后改变某些条件(不改变N2、H2和NH3的用量),反应速率与反应时间的关系如下图,其中表示平衡混合物中NH3的含量最高的一段时间是___________________。当温度为T ℃时,将
2NH3(g)达到平衡后改变某些条件(不改变N2、H2和NH3的用量),反应速率与反应时间的关系如下图,其中表示平衡混合物中NH3的含量最高的一段时间是___________________。当温度为T ℃时,将

(4)合成氨的原料氢气是一种新型的绿色能源,具有广阔的发展前景。现用氢氧燃料电池进行下图所示实验:

①请写出氢氧燃料电池中的电极反应式:
负极:____________________________________________________________;
正极:____________________________________________________________。
②上图装置中,某一铜电极的质量减轻了
(1)分别写出由氧气在一定条件下生成下列物质的化学方程式(注明反应条件):
①O3:_______________________________________________________________________。
②Na2O2:______________________________________________________________________。
③Na2O:______________________________________________________________________。
(2)指出氧元素在下列各物质中的化合价:
O3____________________;K2O2__________________;Na2O__________________________。
(3)RbO2也能吸收CO2放出氧气,其化学方程式是__________________________________。
(4)人体内O-2(超氧离子)对健康有害,使人过早衰老,但在催化剂SOD存在下可发生如下反应,请完成该反应的离子方程式:
![]() O-2+
O-2+ ![]() H2O
H2O![]()
![]() H2O2+
H2O2+![]() O2↑+
O2↑+![]()
![]()
1 mol的某有机物甲在O2中充分燃烧,可得到相同条件下等体积的CO2和H2O(g),并消耗112L(标准状况)O2;又知甲的相对分子质量小于100,1 mol甲在酸性条件下可水解生成1 mol乙和1 mol丙,且丙通过一定途径可转化为乙。
(1)甲的分子式为 。
(2)与甲分子式、所属物质类别都相同的有机物的同分异构体有 种(不含甲)。
|
|
|
②RCH—CHR1 → RCHO+R1CHO
| |
OH OH
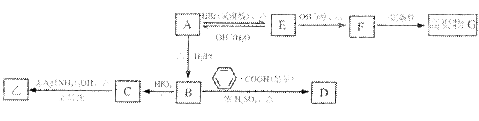 A与甲为同分异构体,且A中含有碳氧双键,B只生成C,与A相关的反应如下:
A与甲为同分异构体,且A中含有碳氧双键,B只生成C,与A相关的反应如下:
(3)写出E→F的反应类型: 。
(4)写出A、G的结构简式:A 、G 。
(5)写出下列转化的反应化学方程式:
B→D ;
C在反应条件为:①下发生反应的化学方程式为 。
(6)A在空气中久置,可转化为相对分子质量为86的化合物H,H的一氯代物只有一种,写出H的结构简式: 。
(4分) 氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4 (1) △H1= -195kJ·mol-1
②N2H4 (1) + O2(g)= N2(g) + 2 H2O △H2= -534.2kJ·mol-1
写出肼和N2O4反应的热化学方程式 ;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com