
题目列表(包括答案和解析)
(12分)反应aA(g)+bB(g) cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
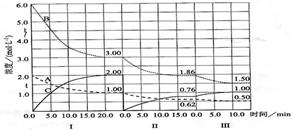
回答问题:
(1)反应的化学方程式中,a:b:c为 ;
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小排列次序为 ;
(3) B的平衡转化率aI(B)、aII(B)、aIII(B)中最小的是 ,其值是 ;
(4)由第一次平衡到第二次平衡,平衡移动的方向是 ,采取的措施是 ;
(5)比较第II阶段反应温度(T1)和第III阶段反应速度(T3)的高低:T2 T3
填“>、=、<”判断的理由是 ;
(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示IV阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C).
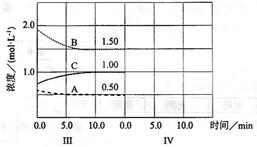
(12分)反应aA(g)+bB(g)cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
回答问题:
(1)反应的化学方程式中,a:b:c为 ;
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小排列次序为 ;
(3) B的平衡转化率aI(B)、aII(B)、aIII(B)中最小的是 ,其值是 ;
(4)由第一次平衡到第二次平衡,平衡移动的方向是 ,采取的措施是 ;
(5)比较第II阶段反应温度(T1)和第III阶段反应速度(T3)的高低:T2 T3
填“>、=、<”判断的理由是 ;
(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示IV阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C).
(12分)反应aA(g)+bB(g) cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
cC(g)(△H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示: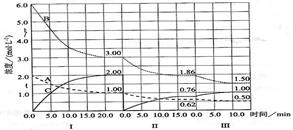
回答问题:
(1)反应的化学方程式中,a:b:c为 ;
(2)A的平均反应速率vI(A)、vII(A)、vIII(A)从大到小排列次序为 ;
(3) B的平衡转化率aI(B)、aII(B)、aIII(B)中最小的是 ,其值是 ;
(4)由第一次平衡到第二次平衡,平衡移动的方向是 ,采取的措施是 ;
(5)比较第II阶段反应温度(T1)和第III阶段反应速度(T3)的高低:T2 T3
填“>、=、<”判断的理由是 ;
(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示IV阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C).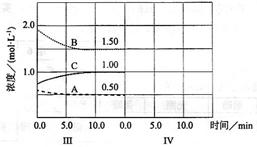
(1)(6 分)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下:
aA (g)+ bB (g) 2C(g)
起始物质的量(mol): 3 2 0
2s末物质的量浓度(mol/L): 0.9 0.8 0.4
则①a= ,b= ;
②2S内B的反应速率= 。
(2)(4分)由碳棒,铁片和200mL 1.5mol/L的稀硫酸组成的原电池中,当在碳棒上产生气体3.36L(标准状况)时,求:
③有 个电子通过了电线?(NA=6.02×1023)
④此时溶液中H+的物质的量浓度为 (不考虑溶液体积变化)。
(3)(2分)将2.3g金属钠放入足量的mg重水(D2O)中,完全反应后,所得溶液中溶质的质量分数是 (用含m的代数式表示)。
(1)(6 分)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下 :
: aA (g)+ bB (g)
aA (g)+ bB (g)  2C(g)
2C(g)  起始物质的量(mol): 3 2 0
起始物质的量(mol): 3 2 0
2s末物质的量浓度(mol/L): 0.9 0.8 0.4
则①a= ,b= ;
②2S内B的反应速率= 。
(2)(4分)由碳棒,铁片和200mL 1.5mol/L的稀硫酸组成的原电池中,当在碳棒上产生气体3.36L(标准状况)时,求:
③有 个电子通过了电线?(NA=6.02×1023)
④此时溶液中H+的物质的量浓度为 (不考虑溶液体积变化)。
(3)(2分)将2.3g金属钠放入足量的mg重水(D2O)中,完全反应后,所得溶液中溶质的质量分数是 (用含m的代数式表示)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com