
题目列表(包括答案和解析)
已知:(1)“欣弗”在酸性条件下可水解生成A( )、B(C9H18SNCl)、C(H3PO4)
)、B(C9H18SNCl)、C(H3PO4)
(2)新型农药甲与A互为同分异构体,甲物质满足以下关系:
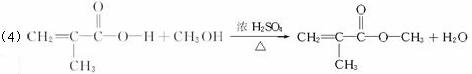
请回答下列问题:
(1)A的分子式为___________________________________________。
(2)甲的结构简式为_________________________________________________。
(3)写出下列各步的反应类型:①___________、④___________。
(4)写出丙生成丁的化学反应方程式____________________________________________。
(08年全国卷Ⅱ)某元素的一种同位素X原子的质量数为A,含N个中子,它与1H原子组成HmX分子,在ag HmX分子中含质子的物质的量是()
A.(A-N+m)mol B.(A-N)mol C. ( A-N)mol D. (A-N+m)mol
(08年全国卷Ⅱ)(13分)某钠盐溶液可能含有阴离子NO3-、CO32-、SO32-、SO42-、Cl-、Br-、I-、为鉴别这些离子,分别取少量溶液进行以下实验:
①测得混合液呈碱性;
②加HCl后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊;
③加CCl4后,滴加少量氯水,振荡后,CCl4后层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
(1)分析上述5个实验,写出每一步实验鉴定离子的结论与理由。
实验① ___________________________ ;
实验② ___________________________ ;
实验③ __________________________;
实验④ ___________________________ ;
实验⑤ ____________________________ ;
(2)上述5个实验不能确定是否存在的离子是 _____ 。
| 化学式 | CaCO3 | CaSO3 | CaC2O4 | Mg(OH)2 |
| Ksp | 4.96×10-9 | 4.96×10-9 | 2.34×10-9 | 5.61×10-12 |
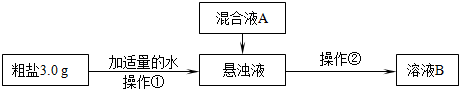
粗盐提纯的研究。
![]() 【有关资料】
【有关资料】
化学式 | CaCO3 | CaSO3 | CaC2O4 | Mg(OH)2 |
Ksp | 4.96×10―9 | 4.96×10―9 | 2.34×10―9 | 5.61×10―12 |
某研究性学习小组对粗盐的提纯和检验进行研究,并提出一些新的方案。已知该粗盐样品中主要含有不溶性杂质、Mg2+、Ca2+等(忽略SO42―的存在),该小组设计流程如下:
![]()

【设计除杂过程】
![]()
![]()
(1)操作①中需要使用的玻璃仪器有 、 。操作②的名称为 ,若在操作②结束后发现溶液B略有浑浊,应采取的措施是_ _____________________________________________________。
(2)混合液A的主要成分是____________________。(填化学式)
【检验除杂效果】
(3)为检验溶液B中Mg2+、Ca2+是否除尽,通常分别取少量溶液B于两支试管中,进行如下实验:
步骤一:检验Mg2+是否除尽。向其中一支试管中加入 溶液(填化学式),看是否有沉淀生成。
步骤二:检验Ca2+是否除尽。向另一支试管中加入某溶液,看是否有沉淀生成。效果最好的是 (填字母)。
A、Na2CO3 B、Na2SO
【获取纯净食盐】
(4)对溶液B加热并不断滴加6 mol?L―1的盐酸溶液,同时用pH试纸检测溶液,直至pH=5时停止加盐酸,得到溶液C。该操作的目的是 。
(5)将溶液C倒入 (填仪器名称)中,加热蒸发并用玻璃棒不断搅拌,直到 ![]() ___________ _____________时(填现象),停止加热。
___________ _____________时(填现象),停止加热。
【问题讨论】
(6)在除杂过程中,向粗盐悬浊液中加混合液A时需要加热,目的是 ,该操作中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在______________以下。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com