
题目列表(包括答案和解析)
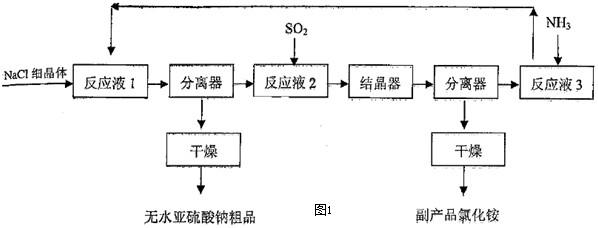
| 原料 | 理论值 | 实际值 | 利用率 |
| SO2 | 50.79 | 54.4 | 93.36% |
| NaCl | 92.86 | 101.0 | 91.94% |
| NH3 | 26.98 | 30.5 | 88.46% |
| 副产品NH4Cl | a | 87.1 | -------- |
项目名称 结果 单位 参考值 ①谷丙转氨酶 7 U/L 40 ②谷草转氨酶 16 U/L 0—40 ③谷酰转肽酶 15 U/L 0—50 ④碱性磷酸酶 77 U/L 34—114 ⑤总胆红素 12.3 μmol·L-1 0—19 ⑥总蛋白 70.6 g·L-1 60—80 ⑦白蛋白 43.9 g·L-1 35—55 ⑧球蛋白 26.7 g·L-1 20—30 ⑨白球比 1.6 1.5—2.5 ⑩乳酸脱氢酶 161 U/L 114—240 ⑾磷酸肌酸激酶 56 U/L 25—200 ⑿甘油三酯 0.52 mmol·L-1 0—1.71 ⒀总胆固醇 4.27 mmol·L-1 3.6—5.18 ⒁高密度脂蛋白胆固醇 1.57 mmol·L-1 1.0—1.6 ⒂低密度脂蛋白胆固醇 1.40 mmol·L-1 0—3.36 ⒃16葡萄糖 4.94 mmol·L-1 3.61—6.11 |
送检日期:2002—09—16 报告日期:2002—09—16 |
其中用物质的量浓度表示的指标有( )
A.①②③④⑩11 B.⑥⑦⑧
C.⑤⑿⒀⒁⒂⒃ D.⑤⑥⑦⑧⑿⒀⒁⒂⒃
(13分)绿矾(化学式FeSO4?7H2O)是硫酸法生产钛白粉的主要副产物,每生产1吨钛白粉,副产4.5~5.0吨绿矾,目前全国每年约副产绿矾75万吨,除极少量被用于制备新产品外,绝大部分作为废料弃去,对环境造成污染。因此开发综合利用绿矾的工艺,是一项很有意义的工作。某研究者提出如下图所示的绿色工艺流程。
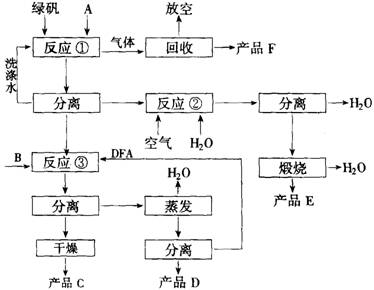
其中A是碳铵,B是氯化物,C是不含氯的优质钾肥,D是一种氮肥,E是红色颜料,F是常见的气体化合物。该工艺实现了原料中各主要成分的利用率均达94% 以上,可望达到综合利用工业废弃物和防治环境污染的双重目的。
9-1 写出B、C、D、E、F的化学式。
9-2 写出反应①、②、③的化学方程式。
9-3 指出反应③需要加入DFA(一种有机溶剂)的理由。
9-4 判断DFA是否溶于水。
(05年全国卷)同一主族的两种元素的原子序数之差不可能是( )
A. 16 B. 26 C. 36 D. 46
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com