(1)一个体重50kg的健康人身体中含铁2g.铁在人体中不是以游离态的形式存在,而是以Fe
2+和Fe
3+形式存在.Fe
2+易被吸收,给贫血者补充铁时,应给予含Fe
2+的盐,如硫酸亚铁(FeSO
4).服用维生素C,可使食物中的Fe
3+转化为Fe
2+,利于铁的吸收,该过程中维生素C做
剂,Fe
3+作
剂,维生素C的还原性
于 Fe
2+(填“强”“弱”)
(2)在热的稀硫酸溶液中溶解了11.4g FeSO
4.当加入50mL 0.5mol/L KNO
3溶液后,使其中的Fe
2+全部转化成Fe
3+,KNO
3也反应完全,并有N
xO
y氮氧化物气体逸出.
FeSO
4+
KNO
3+
H
2SO
4═
K
2SO
4+
Fe
2(SO
4)
3+
N
xO
y+
H
2O
①配平该化学方程式,用单线桥标出电子转移的方向和数目.
②反应中氧化剂为
,氮氧化物的化学式为
.
(3)羟胺(NH
2OH)是一种还原剂,用25.00mL 0.049mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe
2+离子恰好与24.5mL 0.020mol/L的KMnO
4酸性溶液反应.则在上述反应中,Fe
2+离子与酸性高锰酸钾反应的离子方程式为:
.羟胺的氧化产物是
.

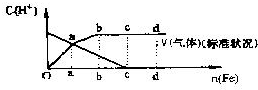 铁在热的稀HNO3中反应,其主要还原产物为N2O,而在冷的稀HNO3中反应,其主要还原产物为NO,当溶液更稀时,其主要还原产物是NH4+.请分析下图,回答有关问题.
铁在热的稀HNO3中反应,其主要还原产物为N2O,而在冷的稀HNO3中反应,其主要还原产物为NO,当溶液更稀时,其主要还原产物是NH4+.请分析下图,回答有关问题.