
题目列表(包括答案和解析)
(1)观察如下反应,总结规律,然后完成下列问题:
①Al(OH)3+H2O Al(OH)4- +H+ ②NH3+H2O
Al(OH)4- +H+ ②NH3+H2O NH4++OH-
NH4++OH-
(A)已知B(OH)3是一元弱酸,试写出其电离方程式
(B)已知N2H4是二元弱碱,试写出其二步电离方程式
。
(2)将a mol Cl2通入含 b mol FeBr2的溶液中,若0<a/b≤1/2时,反应的离子方程式为2Fe2+ +Cl2 = 2Fe3+ +2 Cl-,写出另2个可能发生的离子方程式。
①当1/2< a/b<3/2时 。
②当a/b≥3/2时 。
(1)观察如下反应,总结规律,然后完成下列问题:
①Al(OH)3+H2O Al(OH)4- +H+
②NH3+H2O
Al(OH)4- +H+
②NH3+H2O NH4++OH-
NH4++OH-
(A)已知B(OH)3是一元弱酸,试写出其电离方程式
(B)已知N2H4是二元弱碱,试写出其二步电离方程式
。
(2)将a mol Cl2通入含 b mol FeBr2的溶液中,若0<a/b≤1/2时,反应的离子方程式为2Fe2+ +Cl2 = 2Fe3+ +2 Cl-,写出另2个可能发生的离子方程式。
①当 1/2< a/b<3/2时 。
②当a/b≥3/2时 。
 Al(OH)4- +H+ ②NH3+H2O
Al(OH)4- +H+ ②NH3+H2O NH4++OH-
NH4++OH-(12分)⑴某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应中还原产物是____;若反应过程中转移了0.3moL电子,则氧化产物的质量是__ g。
⑵将a mol Cl2 通入含b mol FeBr2的溶液中,
当0< a / b≤1/2 时,反应的离子方程式为: 2Fe2+ + Cl2 = 2Fe3+ + 2Cl- ,
写出另2个可能发生的离子方程式:
① 当 a / b =1时,_______________________ ______;
② 当a / b≥3/2时,________________ _____________。
⑶观察如下反应,总结规律,然后完成下列问题:
①
Al(OH)3 +H2O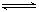 Al(OH)4- + H+
②NH3+H2O
Al(OH)4- + H+
②NH3+H2O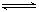 NH4+
+ OH_
NH4+
+ OH_
Ⅰ.已知B(OH)3是一元弱酸,试写出其电离方程式________________________ __
Ⅱ.N2H4是二元弱碱,试写出其第二步电离方程式___________ _________________
(12分)⑴某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应中还原产物是____;若反应过程中转移了0.3moL电子,则氧化产物的质量是__ g。
⑵将a mol Cl2 通入含b mol FeBr2的溶液中,
当0< a / b≤1/2 时,反应的离子方程式为: 2Fe2+ + Cl2 = 2Fe3+ +2Cl- ,
写出另2个可能发生的离子方程式:
① 当 a /b =1时,_______________________ ______;
② 当a /b≥3/2时,________________ _____________。
⑶观察如下反应,总结规律,然后完成下列问题:
① Al(OH)3 +H2OAl(OH)4- + H+ ②NH3+H2O
NH4+ + OH_
Ⅰ.已知B(OH)3是一元弱酸,试写出其电离方程式________________________ __
Ⅱ.N2H4是二元弱碱,试写出其第二步电离方程式___________ _________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com