
题目列表(包括答案和解析)


| A、“神舟六号”返回舱表层用的是具有耐高温、抗氧化的新型无机非金属材料,高温时自动烧蚀带走热量,从而保证内部温度不致过高 | B、“含氟牙膏”、“富硒营养品”中的氟、硒指的是分子,而“高钙牛奶”和“加铁酱油”中指的是钙元素和铁元素 | C、如图为反应物A、B和生成物C的能量示意图,其反应的热化学方程式为:2 A(g)+B(g)═2 C(g)△H=Q kJ?mol-1(Q>0 )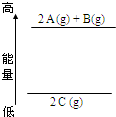 | D、实验室电解水制取氢气和氧气时通常加入硫酸钠等强电解质,目的是增强溶液的导电性 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com